La classification périodique des éléments chimiques
- Fiche de cours
- Quiz et exercices
- Vidéos et podcasts
- Connaitre les critères qui ont permis à Mendeleïev d'établir sa classification.
- Savoir quelle est son utilité pour un chimiste.
- Dans la classification périodique, les éléments sont classés par numéro atomique Z croissant.
- La classification périodique des éléments comporte 7 lignes et 18 colonnes. Les lignes ou périodes représentent le nombre de couches électroniques autour du noyau de l'atome correspondant. Les colonnes représentent le nombres d'électrons sur la couche externe de l'atome.
- Les éléments placés dans une même colonne forment une famille chimique. Ils ont les mêmes propriétés chimiques.
C'est en 1869, que Dimitri Mendeleïev a
proposé la classification périodique des
éléments qui lui permit de regrouper et de
classer tous les atomes connus à cette époque.
Ce classement diffère peu de celui que l'on connait
actuellement.
L'élaboration de cette classification a joué un
grand rôle dans l'évolution des connaissances et
l'avancée de la chimie.
Dimitri Mendeleïev a eu l'idée de classer les éléments connus à l'époque par masse atomique croissante (seul paramètre accesssible à son époque puisque les électrons ne furent mis en évidence que bien plus tard, par J.J. Thomson en 1897).
Son génie réside dans le fait qu'il a prévu une place pour les éléments manquants et qu'il a estimé leur masse. De plus il a remarqué que certains éléments avaient les mêmes propriétés chimiques, anticipant ainsi la notion de famille.
Certains éléments lui ont cependant posé quelques problèmes car il ne savait pas où les placer (par exemple les lanthanides et les gaz nobles).
La classification actuelle regroupe près de 114 éléments, dont 90 naturels (que l'on peut trouver sous forme d'oxyde dans les minerais, etc.).
Les autres sont créés artificiellement au laboratoire et ont parfois une durée de vie très courte (de l'ordre de la microseconde : 10-6 s). Les éléments sont classés par numéro atomique Z croissant et sont regroupés en métaux d'un côté et non-métaux de l'autre.
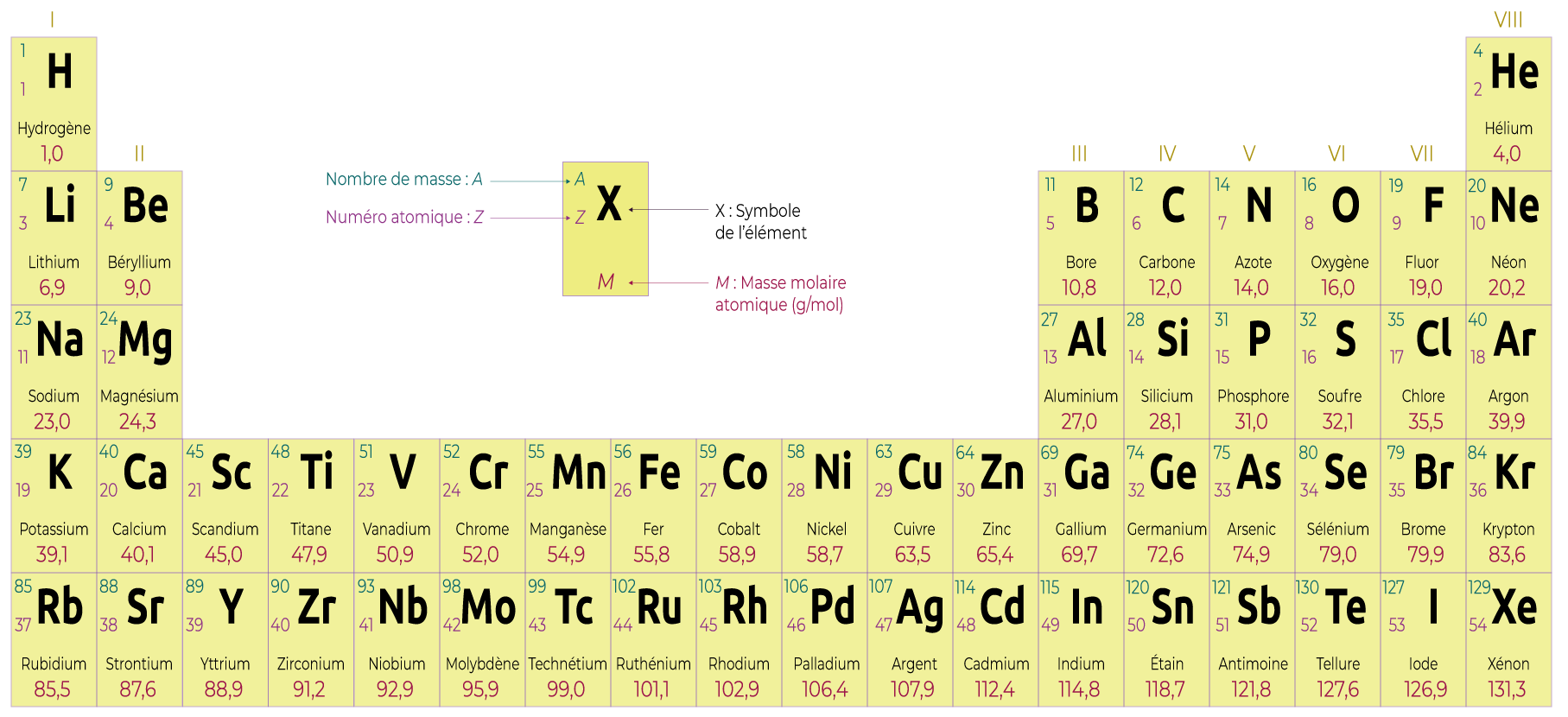
La classification périodique
La classification périodique est un tableau divisé :
- en 7 lignes, appelées périodes ;
- en 18 colonnes qui forment les familles.
Le numéro de la ligne indique le nombre de couches électroniques autour du noyau de l'atome correspondant.
Le numéro de la colonne indique le nombre d'électrons sur la couche externe de l'atome correspondant.
L'atome de carbone
L'élément carbone se situe donc à l'intersection de la 2e ligne (car 2 couches occupées) et de la 4e colonne (car 4 électrons externes)
En fonction de la place de l'élément, la classification permet de connaitre le nombre d'électrons sur la couche externe et le nombre de couches électroniques de l'atome correspondant à l'élément, et réciproquement.
Connaissant le nombre d'électrons externes de l'atome, on peut déterminer le nombre de liaisons covalentes que l'atome établit dans la formation d'une molécule.
Les atomes des éléments situés sur la colonne du carbone (famille du carbone) ont tous 4 électrons sur leur couche externe ; il leur manque donc 4 électrons pour ressembler aux gaz rares les plus proches et vérifier la règle de l'octet. Ils forment donc 4 liaisons covalentes dans une molécule. Les éléments de cette famille sont tétravalents.
On peut aussi en déduire le type d'ions que l'atome va former.
Le fluor F (Z = 9) appartient à la 2e période car l'atome correspondant possède 9 électrons répartis sur 2 couches : (K)2(L)7.
Il appartient à la colonne 17 ou avant-dernière colonne : l'atome correspondant possède 7 électrons externes.
Il lui manque 1 électron pour ressembler au néon Ne (Z = 10) et vérifier ainsi la règle de l'octet.
L'atome de fluor tend donc (comme tous les atomes dont les éléments appartiennent à cette colonne) à gagner 1 électron et former l'ion négatif F– appelé ion fluorure.

Des quiz et exercices pour mieux assimiler sa leçon
La plateforme de soutien scolaire en ligne myMaxicours propose des quiz et exercices en accompagnement de chaque fiche de cours. Les exercices permettent de vérifier si la leçon est bien comprise ou s’il reste encore des notions à revoir.

Des exercices variés pour ne pas s’ennuyer
Les exercices se déclinent sous toutes leurs formes sur myMaxicours ! Selon la matière et la classe étudiées, retrouvez des dictées, des mots à relier ou encore des phrases à compléter, mais aussi des textes à trous et bien d’autres formats !
Dans les classes de primaire, l’accent est mis sur des exercices illustrés très ludiques pour motiver les plus jeunes.

Des quiz pour une évaluation en direct
Les quiz et exercices permettent d’avoir un retour immédiat sur la bonne compréhension du cours. Une fois toutes les réponses communiquées, le résultat s’affiche à l’écran et permet à l’élève de se situer immédiatement.
myMaxicours offre des solutions efficaces de révision grâce aux fiches de cours et aux exercices associés. L’élève se rassure pour le prochain examen en testant ses connaissances au préalable.

Des vidéos et des podcasts pour apprendre différemment
Certains élèves ont une mémoire visuelle quand d’autres ont plutôt une mémoire auditive. myMaxicours s’adapte à tous les enfants et adolescents pour leur proposer un apprentissage serein et efficace.
Découvrez de nombreuses vidéos et podcasts en complément des fiches de cours et des exercices pour une année scolaire au top !

Des podcasts pour les révisions
La plateforme de soutien scolaire en ligne myMaxicours propose des podcasts de révision pour toutes les classes à examen : troisième, première et terminale.
Les ados peuvent écouter les différents cours afin de mieux les mémoriser en préparation de leurs examens. Des fiches de cours de différentes matières sont disponibles en podcasts ainsi qu’une préparation au grand oral avec de nombreux conseils pratiques.

Des vidéos de cours pour comprendre en image
Des vidéos de cours illustrent les notions principales à retenir et complètent les fiches de cours. De quoi réviser sa prochaine évaluation ou son prochain examen en toute confiance !








