Représentation de Lewis de quelques molécules
- Fiche de cours
- Quiz et exercices
- Vidéos et podcasts
Il suffit de suivre un certain nombre d'étapes avant d'accéder à la représentation :
• Dissocier tous les atomes ;
• Donner la configuration électronique de tous les atomes séparés ;
• Repérer combien de liaisons covalentes chaque atome doit réaliser ;
• Faire la somme de tous les électrons externes ;
• Calculer le nombre de doublets à répartir sur la molécule en divisant le nombre d'électrons externes par deux ;
• Répartir les doublets de la molécule en doublets liants (liaisons covalentes) ou en doublets non liants.
Bien entendu, l'édifice chimique imaginé doit être électriquement neutre et chaque atome doit y respecter les règles du duet ou de l'octet. Pour se faire, on peut utiliser des liaisons multiples (double-liaisons covalentes ou triple-liaisons entre atomes).
Elle est constituée de deux atomes d'hydrogène qui contiennent chacun un électron. La répartition électronique est donc : (K)1 ce qui signifie que pour être stable un atome d'hydrogène doit respecter la règle du duet.
ll y a donc en tout 2 électrons externes sur la molécule soit 1 doublet à répartir soit 1 liaison covalente :
• Soit la molécule de chlorure d'hydrogène HCl :
Elle est constituée d'un atome d'hydrogène qui possède 1 électron externe et d'un atome de chlore dont le noyau est noté
L'atome de chlore doit respecter la règle de l'octet et faire une liaison covalente (voir sa structure électronique) et l'hydrogène doit respecter la règle du duet (voir exemple précédent).
• Soit la molécule d'eau H2O :
Elle contient deux atomes d'hydrogène qui ont chacun un électron externe et un atome d'oxygène dont le noyau est noté
Il y a donc en tout 8 électrons externes sur la molécule, soit 4 doublets à répartir :
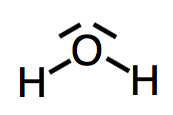
L'oxygène doit faire deux liaisons covalentes (voir sa structure électronique) et respecter la règle de l'octet.
La représentation de Lewis décrit l'enchaînement des atomes, les liaisons covalentes et les doublets non liants de l'édifice moléculaire.

Des quiz et exercices pour mieux assimiler sa leçon
La plateforme de soutien scolaire en ligne myMaxicours propose des quiz et exercices en accompagnement de chaque fiche de cours. Les exercices permettent de vérifier si la leçon est bien comprise ou s’il reste encore des notions à revoir.

Des exercices variés pour ne pas s’ennuyer
Les exercices se déclinent sous toutes leurs formes sur myMaxicours ! Selon la matière et la classe étudiées, retrouvez des dictées, des mots à relier ou encore des phrases à compléter, mais aussi des textes à trous et bien d’autres formats !
Dans les classes de primaire, l’accent est mis sur des exercices illustrés très ludiques pour motiver les plus jeunes.

Des quiz pour une évaluation en direct
Les quiz et exercices permettent d’avoir un retour immédiat sur la bonne compréhension du cours. Une fois toutes les réponses communiquées, le résultat s’affiche à l’écran et permet à l’élève de se situer immédiatement.
myMaxicours offre des solutions efficaces de révision grâce aux fiches de cours et aux exercices associés. L’élève se rassure pour le prochain examen en testant ses connaissances au préalable.

Des vidéos et des podcasts pour apprendre différemment
Certains élèves ont une mémoire visuelle quand d’autres ont plutôt une mémoire auditive. myMaxicours s’adapte à tous les enfants et adolescents pour leur proposer un apprentissage serein et efficace.
Découvrez de nombreuses vidéos et podcasts en complément des fiches de cours et des exercices pour une année scolaire au top !

Des podcasts pour les révisions
La plateforme de soutien scolaire en ligne myMaxicours propose des podcasts de révision pour toutes les classes à examen : troisième, première et terminale.
Les ados peuvent écouter les différents cours afin de mieux les mémoriser en préparation de leurs examens. Des fiches de cours de différentes matières sont disponibles en podcasts ainsi qu’une préparation au grand oral avec de nombreux conseils pratiques.

Des vidéos de cours pour comprendre en image
Des vidéos de cours illustrent les notions principales à retenir et complètent les fiches de cours. De quoi réviser sa prochaine évaluation ou son prochain examen en toute confiance !








