Érosion - dissolution - concrétion
- Fiche de cours
- Quiz et exercices
- Vidéos et podcasts
• Effets mécaniques : le matériau est usé par des chocs répétés avec des grains de matière charriés par les vents (érosion éolienne). Aussi, cela peut concerner l’action mécanique de l’eau, par les vagues, les eaux de ruissellement, ou sous la forme de forces de pression et frottements avec l’avance de glaciers.
• Effets thermiques : le matériau subit de fortes variations de températures, ce qui entraine une alternance de dilatation/compression, d’où l’apparition de fissures. D’autre part, l’action du gel conduit à faire éclater la roche, via l’augmentation de volume de l’eau infiltrée.
• Effets chimiques : des espèces chimiques, dont des acides, vont ronger le matériau.
• Effets biologiques : les racines d’arbres peuvent à la longue s’infiltrer dans les roches, ce qui fragilise ces matériaux. Des microorganismes peuvent s’attaquer à la roche.
Néanmoins, la couverture végétale et une couche de terre protègent également les roches des agressions extérieures. Les racines retiennent les sols. Une roche mise à nue est par contre directement exposée à l’érosion. Dans ce cadre-là, l’action de l’Homme n’est pas négligeable (déforestation).
Un premier stade de l’érosion est la fragmentation mécanique de la roche. Le processus se poursuit alors de plus en plus loin dans le matériau. La fragmentation est accompagnée par une érosion chimique. Elle peut se manifester souvent sous la forme d’une dissolution de la roche (partie 2), mais aussi par une oxydation de la roche, son hydratation, etc. Il en résulte par exemple des sols argileux ou de latérites (roches rouges composées d’oxydes de fer et d’aluminium).
L’eau a un rôle important dans les phénomènes d’érosion. Elle agit selon une action mécanique et chimique. Notamment, le
Les produits de la réaction sont emportés par les rivières, y compris la kaolinite
La première réaction consomme deux moles de
• Anions : Bicarbonate (hydrogénocarbonate)
• Cations : Calcium, Magnésium, Sodium, Potassium, …
Les eaux des rivières sont légèrement salées de part la présence de chlorure de sodium dissous, même si on les désigne sous le terme d’eau douce. Les ions emportés par les rivières arrivent dans les mers et océans.
Edmond Halley (qui étudia aussi la comète qui porte son nom), émit au XVIIème siècle l’hypothèse que la salinité des océans (voir fiche mers océans climats) est due à ce phénomène. Son hypothèse est valide, même si on a trouvé d’autres sources au chlorure de sodium des océans, et des mécanismes faisant que la salinité de l’eau de mer est stable.
Ce qui s’écrit de même selon la réaction globale :
Il s’agit de la réaction inverse de la seconde réaction vue dans la partie 1. C’est ainsi une réaction limitée, dont le sens d’évolution dépend de la concentration des espèces chimiques participantes, et du pH. En effet,
Un sol calcaire érodé est qualifié de karst, en référence à une région de hauts plateaux calcaires typiques de Slovénie. L’érosion du calcaire se caractérise par la formation de structures comme :
• Les gorges : les torrents attaquent le socle calcaire sur lequel ils s’écoulent, dessinant des vallées très encaissées et pentues.
• Les grottes. En progressant dans le sous sol, des cavités souterraines sont creusées dans la roche. L’eau va progresser jusqu’à atteindre une nappe phréatique ou une roche imperméable. Il est courant que l’eau façonne une grotte, puis s’infiltre davantage en profondeur, formant plusieurs étages de grottes.
• Les dolines. Ce sont des dépressions circulaires au niveau du sol, résultant de son affaissement. Comme des sédiments se déposent au fond de la doline, elle abrite une végétation plus abondante qu’aux alentours, un sol calcaire étant peu fertile.
• Les gouffres. La formation des grottes fragilise le sol qui se trouve au-dessus. Il peut localement s’effondrer et former des gouffres.
Les roches sédimentaires sont formées également selon ce principe. On peut citer le calcaire
va évoluer dans le sens direct. En effet, le retrait du
|
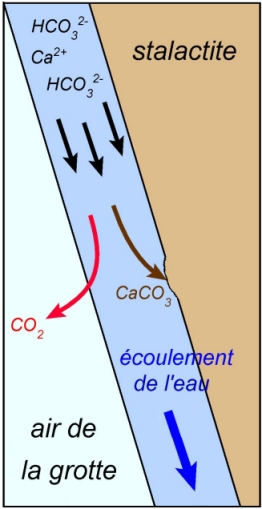
Comme l’humidité de la grotte est forte, l’eau ne s’évapore pas, les gouttes d'eau tombent sous l’effet de la gravité. Les ions restants précipitent également, ce qui crée une structure sous la stalactite : la stalagmite. Elle va progresser vers le plafond de la grotte, jusqu’à rejoindre la stalactite, et former alors une colonne. Le calcaire déposé a une couleur blanc/beige, mais si les eaux emportent également des sels métalliques, les stalactites et stalagmites présentent certaines couleurs : rouge en présence d’oxyde de fer, etc. La vitesse de croissance de ces structures dépend du taux de |
|
L’érosion chimique d’une roche se manifeste principalement par sa dissolution en phase aqueuse. Exemple : eaux minérales, grottes.
La concrétion est une précipitation des ions dissous, afin de former un dépôt solide. Cela peut se faire par évaporation de l’eau (roches sédimentaires) ou par retrait d’un réactif, comme pour la précipitation du calcaire dans les grottes, selon le sens direct de la transformation chimique :
où le

Des quiz et exercices pour mieux assimiler sa leçon
La plateforme de soutien scolaire en ligne myMaxicours propose des quiz et exercices en accompagnement de chaque fiche de cours. Les exercices permettent de vérifier si la leçon est bien comprise ou s’il reste encore des notions à revoir.

Des exercices variés pour ne pas s’ennuyer
Les exercices se déclinent sous toutes leurs formes sur myMaxicours ! Selon la matière et la classe étudiées, retrouvez des dictées, des mots à relier ou encore des phrases à compléter, mais aussi des textes à trous et bien d’autres formats !
Dans les classes de primaire, l’accent est mis sur des exercices illustrés très ludiques pour motiver les plus jeunes.

Des quiz pour une évaluation en direct
Les quiz et exercices permettent d’avoir un retour immédiat sur la bonne compréhension du cours. Une fois toutes les réponses communiquées, le résultat s’affiche à l’écran et permet à l’élève de se situer immédiatement.
myMaxicours offre des solutions efficaces de révision grâce aux fiches de cours et aux exercices associés. L’élève se rassure pour le prochain examen en testant ses connaissances au préalable.

Des vidéos et des podcasts pour apprendre différemment
Certains élèves ont une mémoire visuelle quand d’autres ont plutôt une mémoire auditive. myMaxicours s’adapte à tous les enfants et adolescents pour leur proposer un apprentissage serein et efficace.
Découvrez de nombreuses vidéos et podcasts en complément des fiches de cours et des exercices pour une année scolaire au top !

Des podcasts pour les révisions
La plateforme de soutien scolaire en ligne myMaxicours propose des podcasts de révision pour toutes les classes à examen : troisième, première et terminale.
Les ados peuvent écouter les différents cours afin de mieux les mémoriser en préparation de leurs examens. Des fiches de cours de différentes matières sont disponibles en podcasts ainsi qu’une préparation au grand oral avec de nombreux conseils pratiques.

Des vidéos de cours pour comprendre en image
Des vidéos de cours illustrent les notions principales à retenir et complètent les fiches de cours. De quoi réviser sa prochaine évaluation ou son prochain examen en toute confiance !








