Optimiser une synthèse chimique
- Fiche de cours
- Quiz et exercices
- Vidéos et podcasts
- Identifier, dans un protocole, les opérations réalisées pour optimiser la vitesse de formation d’un produit.
- Comprendre l’augmentation du rendement d’une synthèse par introduction en excès d’un réactif ou par élimination d’un produit du milieu réactionnel.
- Mettre en œuvre un protocole de synthèse pour étudier l’influence de la modification des conditions expérimentales sur le rendement ou la vitesse.
- Pour augmenter le rendement d’une
synthèse, on peut :
- introduire un réactif en large excès ;
- éliminer un produit au fur et à mesure de sa formation.
- Pour optimiser la vitesse d’une réaction,
on peut :
- chauffer la réaction ;
- ajouter un catalyseur.
- Étapes d'un protocole de synthèse
- Facteurs cinétiques, catalyseur
- Réactif, produit, rendement d'une synthèse, taux d’avancement, quotient de réaction et constante d’équilibre
- Montage de la distillation fractionnée
Pour accélérer la vitesse, on peut faire varier :
- la température : en chauffant le milieu réactionnel, on va pouvoir accélérer la réaction chimique ;
- la concentration d’un réactif : plus la concentration d’un ou de plusieurs réactifs est grande, plus la réaction évolue rapidement. À l’opposé, plus les réactifs sont dilués, plus la réaction est lente.
- Un catalyseur permet d’accélérer une réaction sans être consommé. Un catalyseur n’est toutefois pas un facteur cinétique car ce n’est pas un paramètre, mais une espèce chimique.
- Le catalyseur ne figure pas dans l’équation de la réaction ; il n’influence pas le sens d’évolution de la transformation, ni la composition du système dans l’état final.
Le rendement se note η et s’exprime par la relation suivante.
|
|
avec :
|
Le rendement est une valeur comprise entre 0 et 1. Il peut aussi s’exprimer en pourcentage.
L’optimisation d’une synthèse chimique repose sur plusieurs points.
- Minimiser le temps de la manipulation en accélérant la réaction, car certaines réactions peuvent être très lentes.
- Obtenir un rendement le plus élevé possible pour obtenir un maximum de produit.
On va étudier les techniques d’optimisation d’une synthèse chimique en étudiant l’influence des conditions expérimentales. On s’intéresse ici à l’exemple de la synthèse d’un ester, l’estérification.
La synthèse d’un ester consiste à faire réagir deux réactifs :
- un alcool qui contient le groupe hydroxyle —OH ;
- un acide carboxylique qui contient le groupe
carboxyle
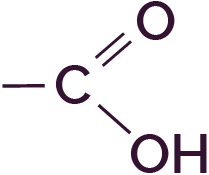 .
.
On obtient alors une nouvelle molécule qui
contient le groupe caractéristique ester
![]() .
.
Pour cette synthèse, on fait réagir :
- le 3-méthylbutan-1-ol de formule
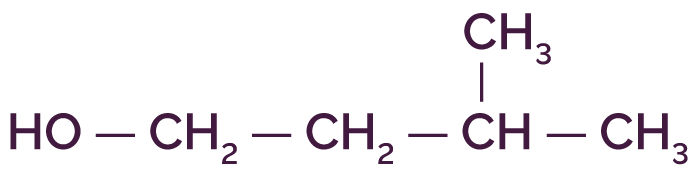 ;
;
- l’acide éthanoïque de formule
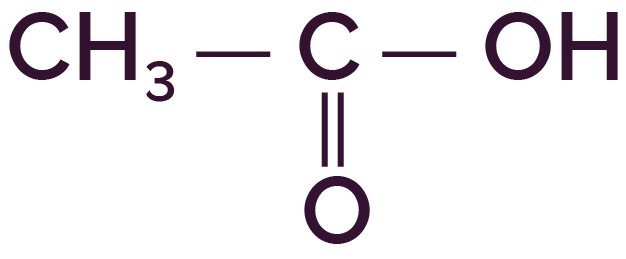 .
.
L’équation de la réaction s’écrit de la manière suivante.
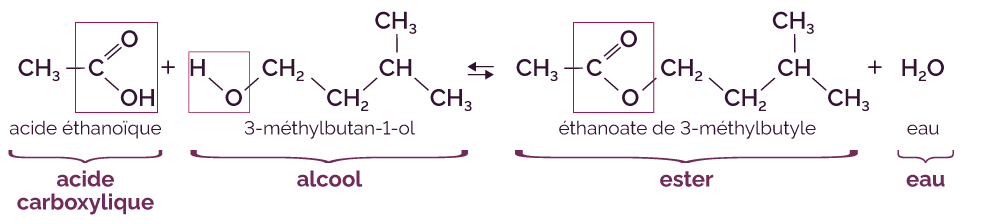
Réaction chimique de la synthèse de l’ester
Cette réaction se déroule dans les deux sens. La réaction qui a lieu en sens inverse entre l'ester et l'eau est appelée « hydrolyse de l'ester » et se produit simultanément à la synthèse de l’ester. La réaction d’estérification se produit lentement et elle est limitée par la réaction inverse de l’hydrolyse de l’ester. On cherche donc à optimiser cette réaction.
On cherche à étudier l’influence de deux paramètres sur la vitesse de réaction de la synthèse d’un ester : la température et l’utilisation d’un catalyseur.
On effectue deux expériences au cours desquelles on met en contact les deux réactifs à deux températures différentes T1 et T2, avec T1 > T2.
On trace ensuite la courbe qui représente la quantité de matière d’ester formée en fonction du temps.
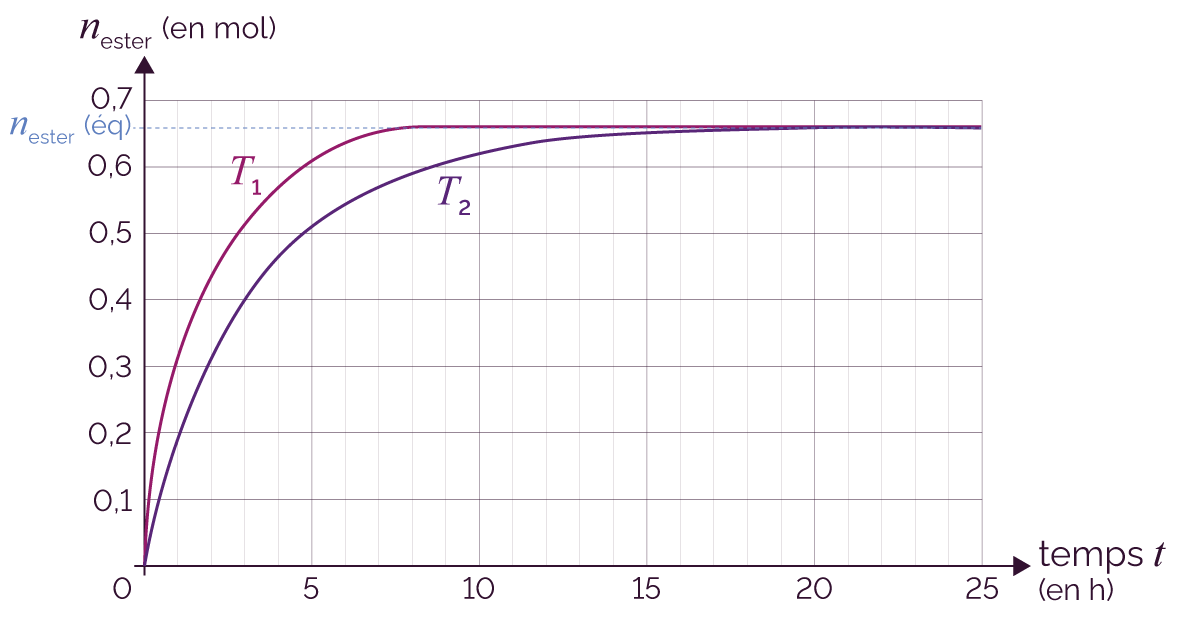
Courbe des résultats avec deux températures différentes
Observation et conclusion
L’état d’équilibre est atteint plus rapidement avec la courbe de température la plus élevée.
On utilise le plus souvent l’acide sulfurique pour catalyser la réaction (il contient les ions oxonium H3O+).
On effectue deux expériences au cours desquelles on met en contact les deux réactifs en présence d’un catalyseur et sans catalyseur.
On trace ensuite la courbe qui représente la quantité de matière d’ester formée en fonction du temps.
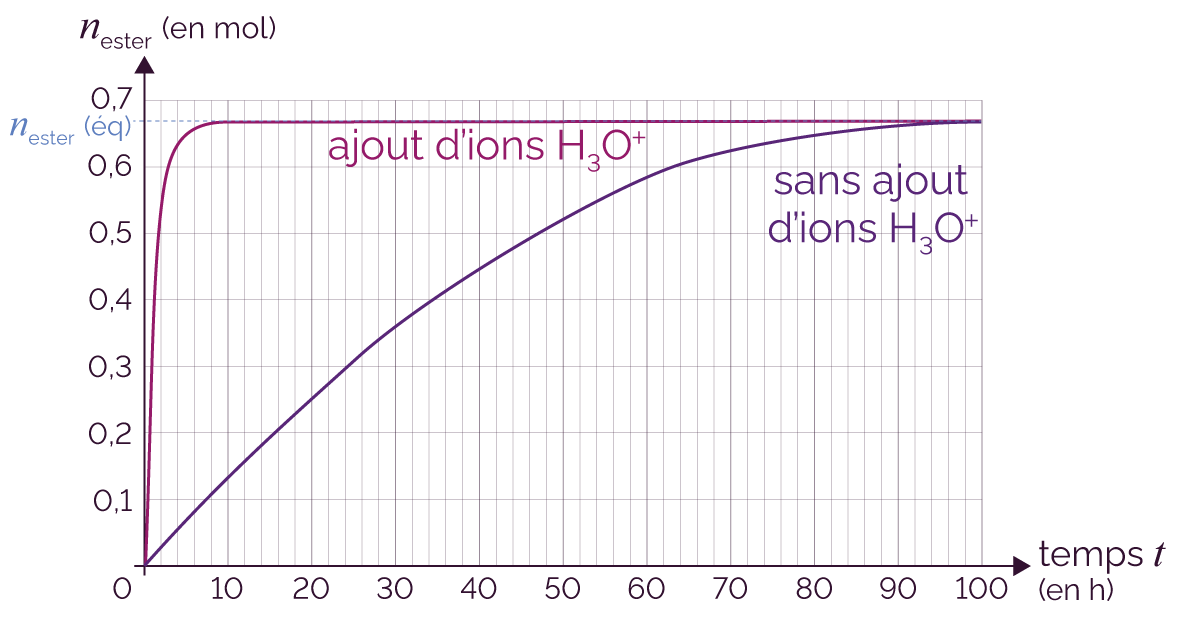
Courbe des résultats avec et sans catalyseur
Observation et conclusion
L’état d’équilibre est atteint plus rapidement avec un catalyseur.
Le rendement de l'estérification est le rapport entre la quantité de matière d'ester obtenue expérimentalement et la quantité de matière d'ester que l'on obtiendrait si la réaction était totale (nester max) :
![]() .
.
Le rendement de la réaction d’estérification peut être optimisé en jouant sur la composition initiale, et/ou en éliminant un produit au fur et à mesure de sa formation.
On réalise diverses réactions d’estérification au cours desquelles on modifie les quantités initiales des réactifs introduits (acide éthanoïque et 3-méthylbutan-1-ol).
On regroupe les résultats dans le tableau suivant.
| n(ac)i (en mol) | 5 | 2 | 1 | 1 | 1 |
| n(al)i (en mol) | 1 | 1 | 1 | 2 | 5 |
|
η (sans unité) |
0,35 | 0,31 | 0,25 | 0,31 | 0,35 |
On a noté n(ac)i et n(al)i les quantités initiales d’acides et d’alcool introduites, et η le rendement de la réaction.
Observation
Le rendement est maximal lorsque l’un des
réactifs est introduit en large excès par
rapport à l’autre.
Interprétation
L’expression du quotient de la réaction de
synthèse de l’ester est :
![]()
L’expression de la constante d’équilibre vaut :
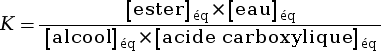
On observe que l’eau est présente dans les expressions du quotient de la réaction et de la constante d’équilibre. Cela s’explique par le fait que l’eau n’est pas le solvant mais un produit de la réaction.
On suppose qu’on a atteint l’état d’équilibre : Qr = K.
On ajoute ensuite un excès de réactif, l’acide par exemple : on a alors n(acide) > n(acide)éq, ce qui implique que Qr < K car la constante de la réaction est inversement proportionnelle à la concentration en acide.
Le système va alors évoluer de sorte à ce que le quotient de la réaction Qr tende vers la constante d’équilibre K : il faut donc éliminer l’espèce ajoutée (l’acide) en la consommant, donc en favorisant la production d’ester.
Conclusion
On suppose qu’on a atteint l’état d’équilibre : Qr = K.
On élimine ensuite l’un des produits, l’eau par exemple : on a alors n(eau) < n(eau)éq, ce qui implique Qr < K.
Le système va alors évoluer de sorte à ce que le quotient de la réaction Qr tende vers la constante d’équilibre K : il faut donc produire l’espèce éliminée en favorisant la production d’ester.
Conclusion
En retirant un produit au fur et à mesure de sa formation, on empêche la réaction inverse (hydrolyse de l’ester) de se réaliser. Il n’y a qu’une seule réaction qui se produit, celle de la synthèse de l’ester dans le sens direct, ce qui permet d’augmenter son rendement.
Pour optimiser la vitesse et le rendement d’une réaction, il faut faire en sorte de respecter les trois points suivants :
- chauffer le milieu réactionnel ;
- utiliser un catalyseur ;
- utiliser un montage qui permet d’éliminer un produit au fur et à mesure de sa formation.
Afin de respecter ces trois points, on utilise un
montage de distillation fractionnée en
présence d’un catalyseur :
l’acide sulfurique
H2SO4.
Il faut donc procéder de la manière
suivante.
- Prélever les réactifs (acide éthanoïque et 3-méthylbutan-1-ol), puis les mettre en contact dans le ballon afin qu’ils interagissent.
- Ajouter quelques gouttes d’acide sulfurique.
- Réaliser le montage de distillation fractionnée.
- Mettre en route le chauffe ballon.
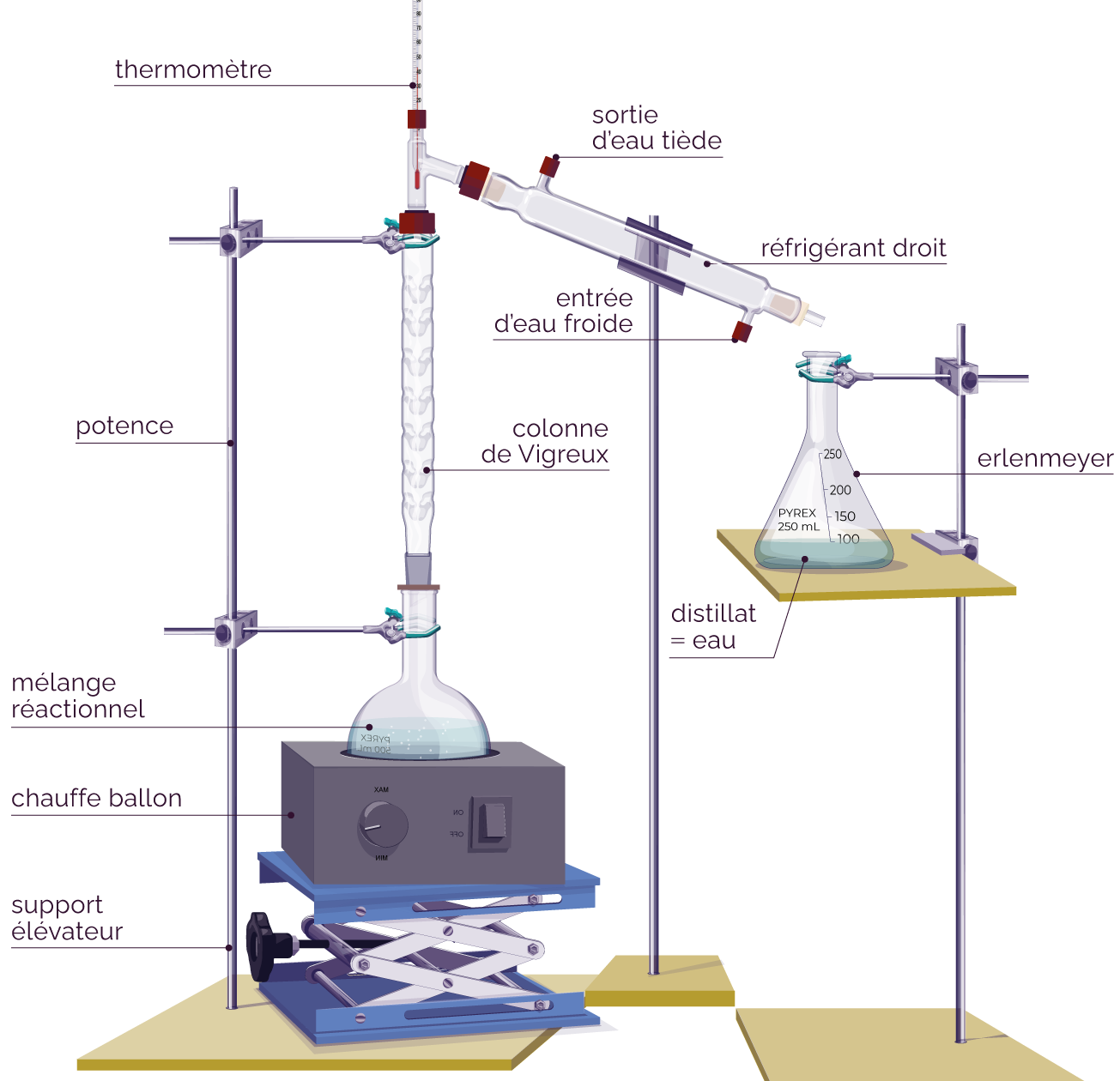
Montage de la distillation fractionnée
de la synthèse de l’ester
Le montage permet de porter à ébullition
un mélange de liquides miscibles dotés de
températures d’ébullition
différentes afin d’extraire le liquide qui
a la plus faible température
d’ébullition.
Pour savoir quelle espèce chimique a la
température d’ébullition la plus
faible, on étudie le tableau suivant.
|
Températures d'ébullition |
eau | 100 °C |
| acide éthanoïque | 118 °C | |
| 3-méthylbutan-1-ol | 131 °C | |
| éthanoate de 3-méthylbutyle | 142 °C |
Dans la réaction d’estérification, on remarque que l’eau possède la température d’ébullition la plus faible. C’est donc l’eau qui sera éliminée au fur et à mesure de sa formation dans ce montage. Il s’agit d’un produit de cette réaction de synthèse d’ester, le rendement va donc augmenter.

Des quiz et exercices pour mieux assimiler sa leçon
La plateforme de soutien scolaire en ligne myMaxicours propose des quiz et exercices en accompagnement de chaque fiche de cours. Les exercices permettent de vérifier si la leçon est bien comprise ou s’il reste encore des notions à revoir.

Des exercices variés pour ne pas s’ennuyer
Les exercices se déclinent sous toutes leurs formes sur myMaxicours ! Selon la matière et la classe étudiées, retrouvez des dictées, des mots à relier ou encore des phrases à compléter, mais aussi des textes à trous et bien d’autres formats !
Dans les classes de primaire, l’accent est mis sur des exercices illustrés très ludiques pour motiver les plus jeunes.

Des quiz pour une évaluation en direct
Les quiz et exercices permettent d’avoir un retour immédiat sur la bonne compréhension du cours. Une fois toutes les réponses communiquées, le résultat s’affiche à l’écran et permet à l’élève de se situer immédiatement.
myMaxicours offre des solutions efficaces de révision grâce aux fiches de cours et aux exercices associés. L’élève se rassure pour le prochain examen en testant ses connaissances au préalable.

Des vidéos et des podcasts pour apprendre différemment
Certains élèves ont une mémoire visuelle quand d’autres ont plutôt une mémoire auditive. myMaxicours s’adapte à tous les enfants et adolescents pour leur proposer un apprentissage serein et efficace.
Découvrez de nombreuses vidéos et podcasts en complément des fiches de cours et des exercices pour une année scolaire au top !

Des podcasts pour les révisions
La plateforme de soutien scolaire en ligne myMaxicours propose des podcasts de révision pour toutes les classes à examen : troisième, première et terminale.
Les ados peuvent écouter les différents cours afin de mieux les mémoriser en préparation de leurs examens. Des fiches de cours de différentes matières sont disponibles en podcasts ainsi qu’une préparation au grand oral avec de nombreux conseils pratiques.

Des vidéos de cours pour comprendre en image
Des vidéos de cours illustrent les notions principales à retenir et complètent les fiches de cours. De quoi réviser sa prochaine évaluation ou son prochain examen en toute confiance !








