Déterminer les isotopes radioactifs à partir du diagramme (N, Z)
- Fiche de cours
- Quiz et exercices
- Vidéos et podcasts
- Déterminer les isotopes radioactifs d’un élément à partir d’un diagramme (N, Z).
- Utiliser des données pour identifier le type de radioactivité.
- La radioactivité est le phénomène au cours duquel un noyau instable (appelé noyau radioactif) se désintègre spontanément en un noyau qui appartient à un autre élément chimique.
- La désintégration radioactive s’accompagne de l’émission d’une particule et d’un rayonnement électromagnétique gamma.
- Le diagramme (N, Z) répertorie tous les isotopes instables et stables de tous les éléments chimiques. On trouve en abscisse le nombre de neutrons et en ordonnée le nombre de protons.
- Il existe trois types de radioactivité en
fonction de la particule émise :
- la radioactivité béta plus correspond à l’émission d’un positon ;
- la radioactivité béta moins correspond à l’émission d’un électron ;
- la radioactivité alpha correspond à l’émission d’un noyau d’hélium 4.
- Tous les isotopes se trouvent sur une même ligne sur le diagramme (N, Z).
- Les isotopes
- La réaction nucléaire
La radioactivité est un phénomène physique qui concerne des noyaux instables qui se désintègrent. Cette désintégration est à la fois aléatoire (on ne peut pas prévoir quand elle va avoir lieu) et spontanée (elle se réalise sans intervention extérieure).
Le rayonnement gamma (γ) émis lors de la désintégration radioactive est un rayonnement électromagnétique de courte longueur d’onde (l’ordre de grandeur est λ = 10–12 m).
Le noyau qui se désintègre est appelé noyau père et le noyau formé est appelé noyau fils.
Un noyau est composé de protons (portant une charge électrique élémentaire positive) et de neutrons (électriquement neutres).
L’élément chimique auquel appartient le noyau est défini par le nombre de charges Z (qui est égal au nombre de protons) et on définit le nombre de masse A du noyau qui est égal à la somme des protons et des neutrons.

On nomme des isotopes en donnant le nom de l’élément chimique auxquels ils appartiennent suivi de la valeur du nombre de masse A, ou en utilisant la notation AX.
Le carbone 14 (14C) se désintègre en se transformant en azote 14 (14N) et en émettant un électron.
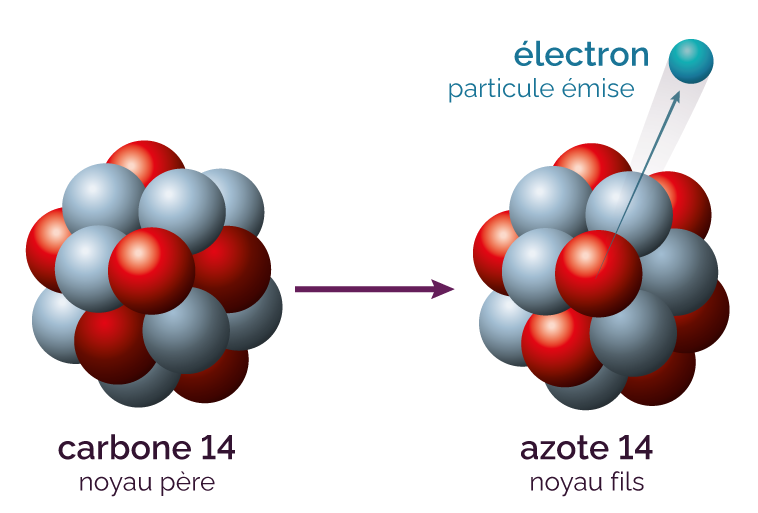
La désintégration radioactive du carbone 14
En fonction de la nature de la particule émise, on distingue trois types de radioactivité : béta plus, béta moins et alpha.
| Type de radioactivité | Particule émise | Symbole de la particule |
| Béta moins (β–) | Électron |

|
| Béta plus (β+) | Positon |

|
| Alpha (α) | Noyau d’hélium 4 |

|
Un noyau de carbone 14 se désintègre spontanément en un noyau d’azote 14 avec l’émission d’un électron et d’un rayonnement gamma : c’est donc une radioactivité de type béta moins (β–).
Les noyaux avec un excès de protons se désintègrent selon la radioactivité β+ en émettant un positon (
Les noyaux lourds avec un excès de nucléons se désintègrent selon la radioactivité α en émettant un noyau d’hélium 4 (
Le diagramme (N, Z) répertorie pour chaque élément chimique les isotopes stables et ceux qui sont instables (radioactifs).
Dans ce diagramme, le nombre de neutrons N (égal à A – Z) se trouve en abscisse et le nombre de protons (égal à Z) se trouve en ordonnée.
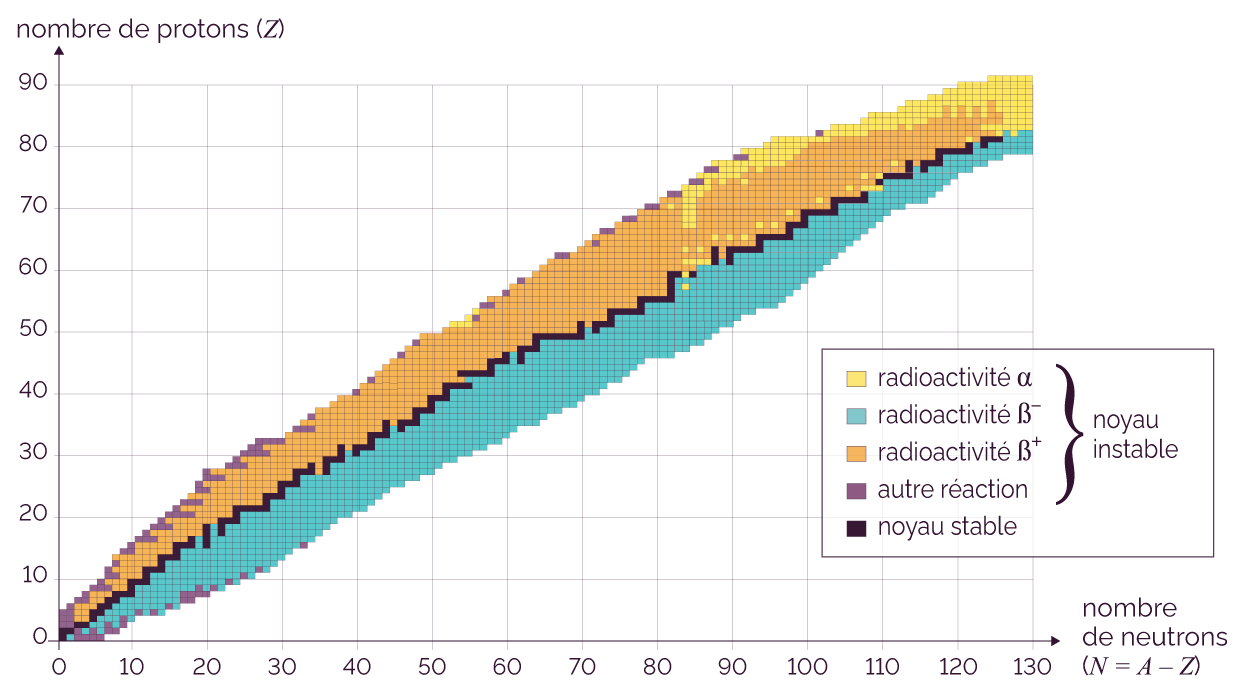
Diagramme (N, Z)
Ce diagramme permet d’identifier, pour un élément chimique donné, les isotopes stables et les isotopes instables.
On identifie des isotopes stables et instables du bismuth (Z = 83), à partir d’un extrait du diagramme (N, Z).
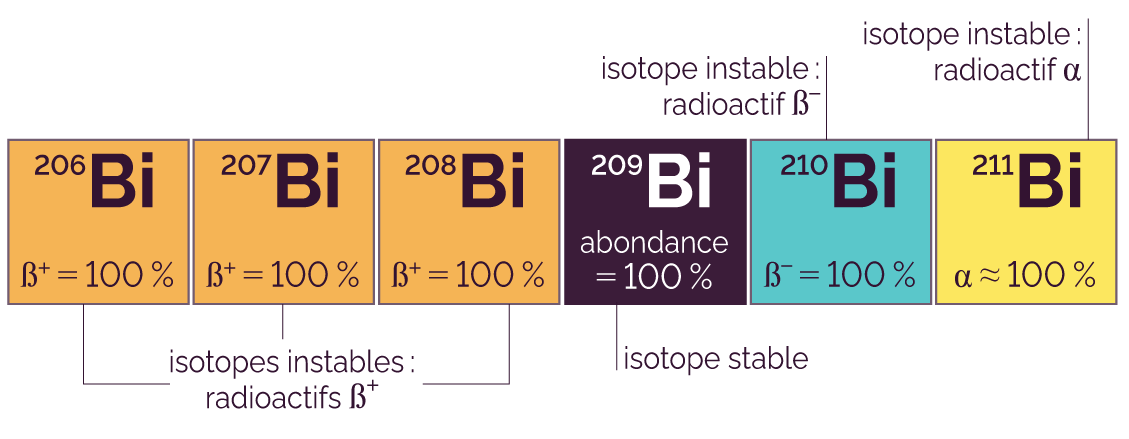
Pour les isotopes radioactifs, le type de radioactivité associée (β–, β+ ou α) nous permet de trouver le noyau fils à partir du diagramme (N, Z).
| Type de radioactivité |
Variation du nombre de protons et de neutrons entre les noyaux père et fils |
Déplacement dans le diagramme (N, Z) |
| Béta moins (β–) |
Un proton en plus, un neutron en moins |
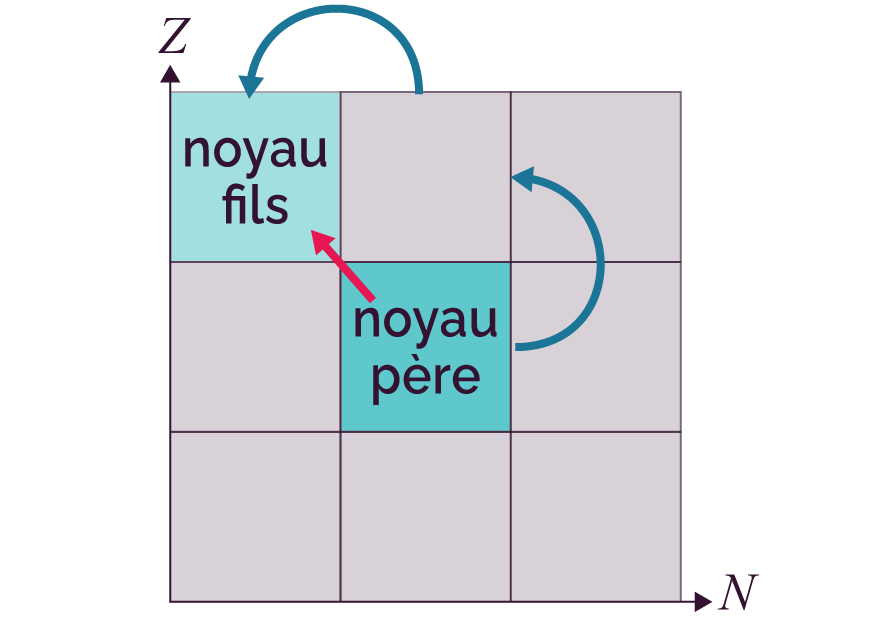
|
| Béta plus (β+) |
Un proton en moins, un neutron en plus |
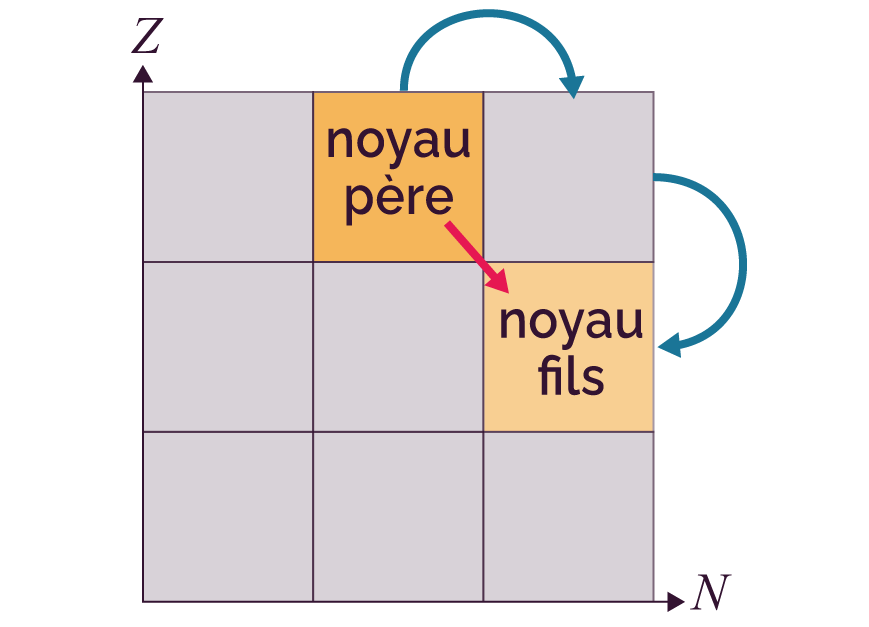
|
| Alpha (α) |
Deux protons en moins, deux neutrons en moins |
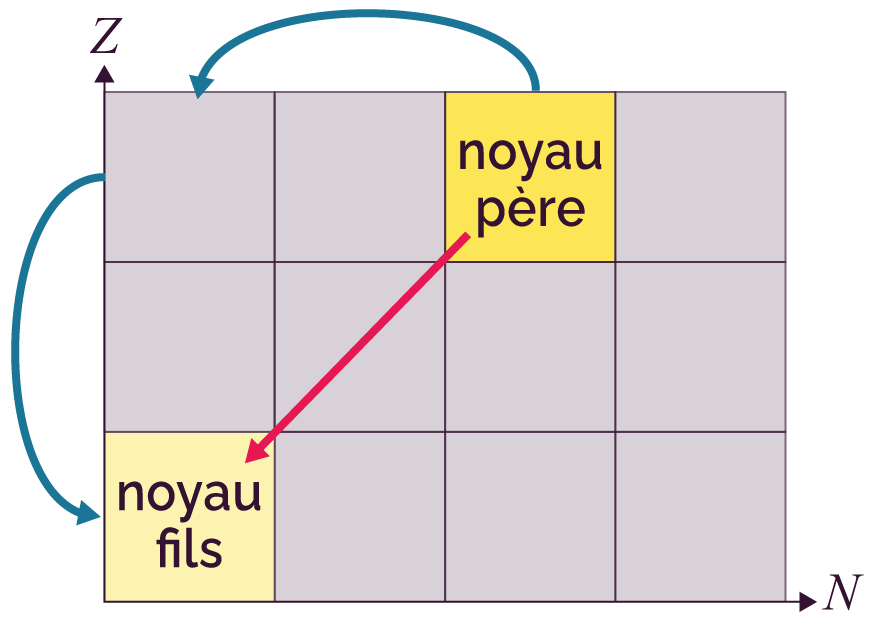
|
La variation du nombre de protons et de neutrons s’obtient à partir des lois de conservation au cours de la réaction nucléaire.

Des quiz et exercices pour mieux assimiler sa leçon
La plateforme de soutien scolaire en ligne myMaxicours propose des quiz et exercices en accompagnement de chaque fiche de cours. Les exercices permettent de vérifier si la leçon est bien comprise ou s’il reste encore des notions à revoir.

Des exercices variés pour ne pas s’ennuyer
Les exercices se déclinent sous toutes leurs formes sur myMaxicours ! Selon la matière et la classe étudiées, retrouvez des dictées, des mots à relier ou encore des phrases à compléter, mais aussi des textes à trous et bien d’autres formats !
Dans les classes de primaire, l’accent est mis sur des exercices illustrés très ludiques pour motiver les plus jeunes.

Des quiz pour une évaluation en direct
Les quiz et exercices permettent d’avoir un retour immédiat sur la bonne compréhension du cours. Une fois toutes les réponses communiquées, le résultat s’affiche à l’écran et permet à l’élève de se situer immédiatement.
myMaxicours offre des solutions efficaces de révision grâce aux fiches de cours et aux exercices associés. L’élève se rassure pour le prochain examen en testant ses connaissances au préalable.

Des vidéos et des podcasts pour apprendre différemment
Certains élèves ont une mémoire visuelle quand d’autres ont plutôt une mémoire auditive. myMaxicours s’adapte à tous les enfants et adolescents pour leur proposer un apprentissage serein et efficace.
Découvrez de nombreuses vidéos et podcasts en complément des fiches de cours et des exercices pour une année scolaire au top !

Des podcasts pour les révisions
La plateforme de soutien scolaire en ligne myMaxicours propose des podcasts de révision pour toutes les classes à examen : troisième, première et terminale.
Les ados peuvent écouter les différents cours afin de mieux les mémoriser en préparation de leurs examens. Des fiches de cours de différentes matières sont disponibles en podcasts ainsi qu’une préparation au grand oral avec de nombreux conseils pratiques.

Des vidéos de cours pour comprendre en image
Des vidéos de cours illustrent les notions principales à retenir et complètent les fiches de cours. De quoi réviser sa prochaine évaluation ou son prochain examen en toute confiance !








