Réaliser une pile
- Fiche de cours
- Quiz et exercices
- Vidéos et podcasts
- Modéliser et schématiser, à partir de résultats expérimentaux, le fonctionnement d’une pile.
- Réaliser une pile, déterminer sa tension à vide et la polarité des électrodes, identifier la transformation mise en jeu, illustrer le rôle du pont salin.
- Une réaction d’oxydoréduction correspond à un transfert d’électrons entre deux réactifs (un oxydant et un réducteur).
- Ce transfert est direct si l’oxydant et le réducteur sont en contact, ou alors il peut s’effectuer par un circuit extérieur si les réactifs ne sont pas en contact : on a alors une pile.
- La mesure de la tension aux bornes de la pile permet de trouver sa polarité. Lorsque la pile ne fournit pas de courant, cette tension est appelée tension à vide.
- Le pont salin (composé d’une solution aqueuse ionique gélifiée) relie les deux demi-piles et permet d’assurer la circulation du courant dans la pile.
- La mesure d’une tension électrique
- La réaction d’oxydoréduction
- Étudier le fonctionnement d’une pile
Une réaction d’oxydoréduction correspond à un transfert d’électrons entre deux entités chimiques. L’oxydant capte un ou plusieurs électrons qui sont cédés par le réducteur. Cette réaction est à l’origine de la production d’énergie dans une pile lorsque les électrons sont récupérés et circulent dans un circuit extérieur à la pile.
On place une plaque métallique M2
dans un bécher qui contient une solution aqueuse
avec un ion métallique M1![]() .
.

Étude de la réaction entre un métal
et un cation métallique
On observe l’état du système au bout de quelques heures et on identifie si une réaction a eu lieu ou pas.
| Métal | Cation | Observations | Équation de réaction |
| Zinc Zn | Cu2+ | Réaction | Cu2+ (aq) + Zn (s) → Cu (s) + Zn2+ (aq) |
| Cuivre Cu | Zn2+ | Pas de réaction | |
| Argent Ag | Cu2+ | Pas de réaction | |
| Cuivre Cu | Ag+ | Réaction | 2 Ag+ (aq) + Cu (s) → 2 Ag (s) + Cu2+ (aq) |
Les expériences où une réaction a eu lieu correspondent à un transfert direct d’électrons entre le métal réducteur et le cation métallique oxydant : en se transformant en cation métallique, le métal cède des électrons au cation métallique déjà présent qui se transforme en métal.
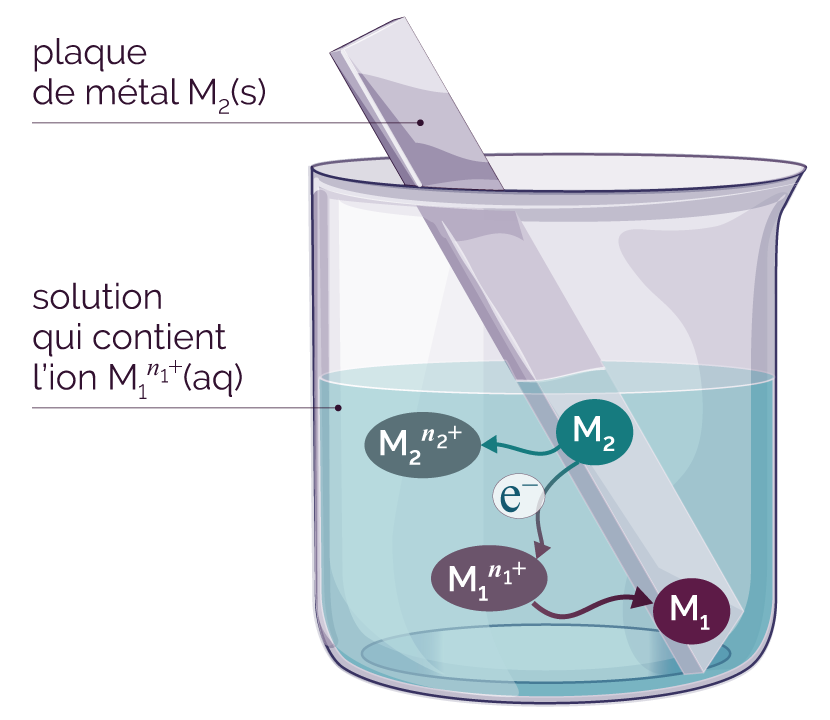
Illustration du transfert direct d’électrons
Lors d’un transfert direct d’électrons, ceux-ci ne sont pas récupérés pour être utilisés dans un circuit électrique. Cela ne constitue pas une pile.
En revanche, le métal M2 va
être oxydé par les
ions M1![]() . Il y a donc un
phénomène de corrosion.
. Il y a donc un
phénomène de corrosion.
Les ions M1
On prépare deux béchers qui contiennent
chacun une plaque métallique (M1
ou M2), appelée aussi
électrode, qui plonge dans une solution aqueuse
contenant l’ion métallique associé
(M1![]() ou
M2
ou
M2![]() ).
).
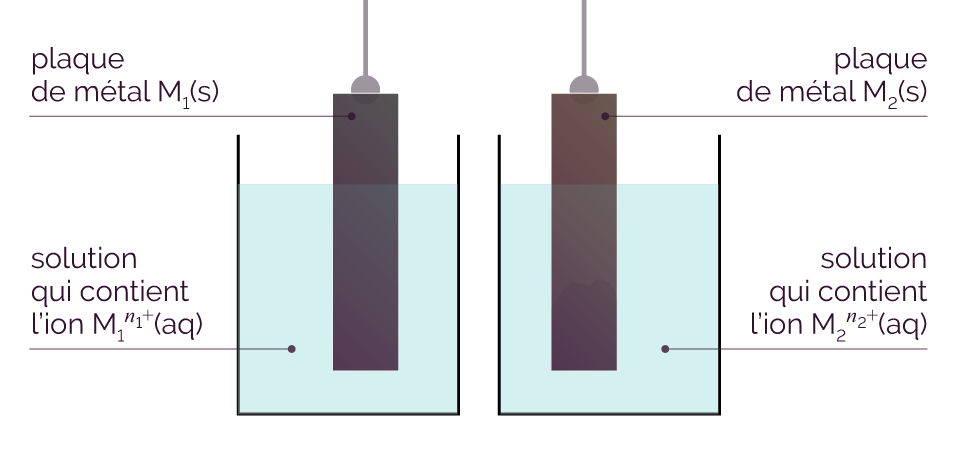
Dispositif expérimental d'étude
On relie les deux plaques par un circuit métallique conducteur.
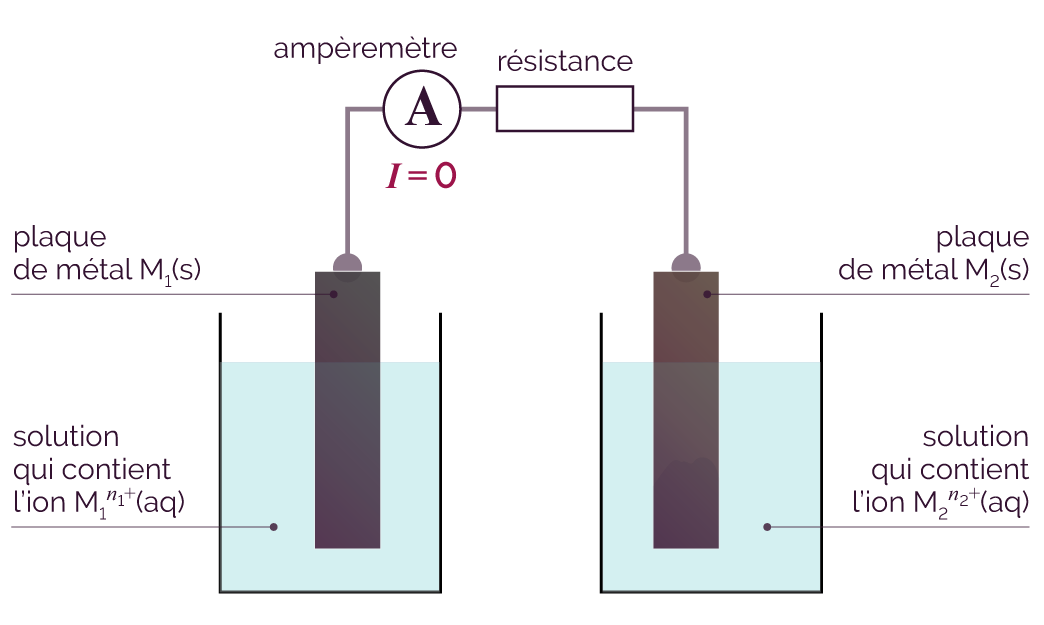
Connexion entre les deux plaques
L’ampèremètre branché dans le circuit mesure une intensité nulle : aucun courant ne circule car le circuit est ouvert (pas de connexion entre les deux béchers).
On relie maintenant les deux solutions contenues dans les béchers par un pont salin (tube en forme de U contenant une solution aqueuse gélifiée ionique).
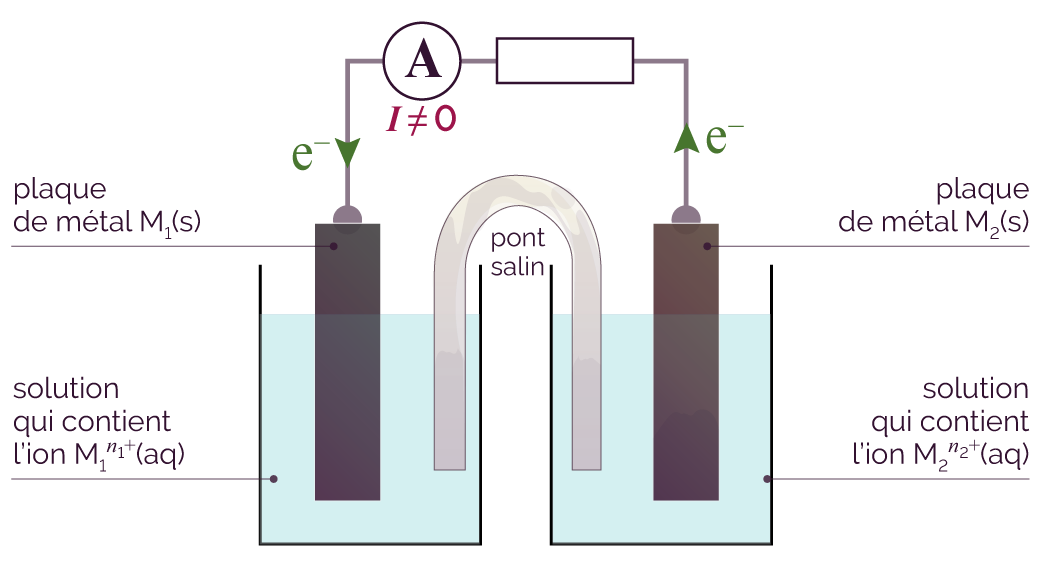
Connexion avec le pont salin
L’ampèremètre branché dans le circuit mesure une intensité non nulle : un courant électrique circule.
Des électrons sont transférés de la plaque où le métal réagit en s’oxydant, vers la plaque ou le cation métallique réagit en se réduisant.
L’équation chimique de la réaction observée à chaque électrode est la suivante.
- Électrode M1 :
M1
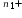 (aq) + n1e–
→ M1 (s)
(aq) + n1e–
→ M1 (s)
- Électrode M2 : M2
(s) →
M2
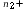 (aq) + n2e–
(aq) + n2e–
L’équation associée au fonctionnement du système élaboré est la suivante.
n2 × M1![]() (aq)
+ n1 ×
M2 (s) → n2 ×
M1 (s) +
n1 ×
M2
(aq)
+ n1 ×
M2 (s) → n2 ×
M1 (s) +
n1 ×
M2![]() (aq)
(aq)
Il s’agit de la même équation que
celle que l’on obtiendrait si le
métal M2 et le cation
métallique M1![]() avait
été en contact.
avait
été en contact.
Le système élaboré permet de faire passer un courant électrique qui assure le transfert indirect des électrons entre les réactifs qui ne sont pas en contact. Il transforme une énergie chimique en une énergie électrique : c’est le principe de la pile électrochimique.
On réalise une pile argent-zinc en réunissant :
- une demi-pile composée d’une plaque de zinc Zn (appelée électrode) qui plonge dans une solution contenant l’ion zinc (II) Zn2+ ;
- une demi-pile composée d’une plaque d’argent Ag (appelée électrode) qui plonge dans une solution contenant l’ion argent Ag+.
La masse de chacune des deux plaques est égale à 50 g et les concentrations en quantité de matière en ion zinc (II) et en ion argent sont égales à 0,10 mol·L–1.
On relie les deux demi-piles avec un pont salin qui
contient une solution aqueuse gélifiée de
nitrate d’ammonium, contenant les ions nitrate
NO![]() et les ions ammonium NH
et les ions ammonium NH![]() .
.
On relie les deux demi-piles avec un pont salin.
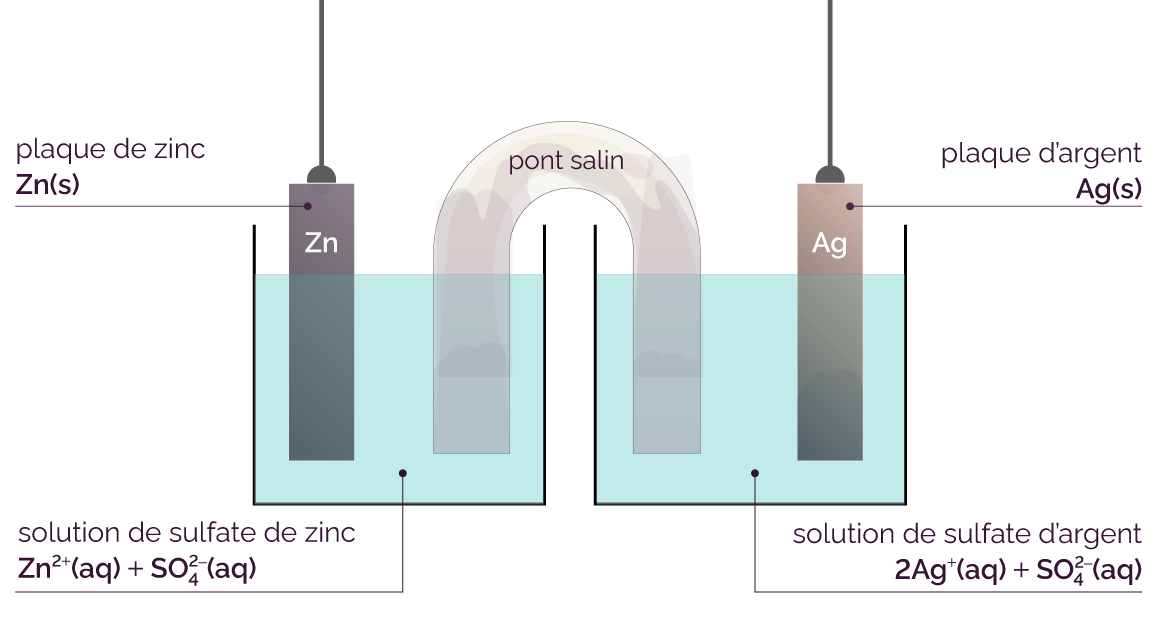
Pile zinc-argent
On branche aux bornes de cet ensemble un voltmètre qui permet de mesurer la tension à vide de la pile et ainsi de déterminer la polarité de celle-ci.

Mesure de la tension à vide
Le signe de la tension mesurée permet d’identifier le signe des électrodes branchées aux bornes du voltmètre.
| Signe de la tension mesurée |
Signe de
l’électrode reliée à V |
Signe de
l’électrode reliée à COM |
| Positif | Positif | Négatif |
| Négatif | Négatif | Positif |
La tension mesurée est ici négative, on en déduit que la plaque branchée sur la borne V est négative et que la plaque branchée sur la borne COM est positive.
L’électrode de zinc constitue le pôle négatif de la pile (anode) et l’électrode d’argent constitue le pôle positif (cathode).
On branche désormais un circuit aux bornes de la pile, et on mesure l’intensité du courant.
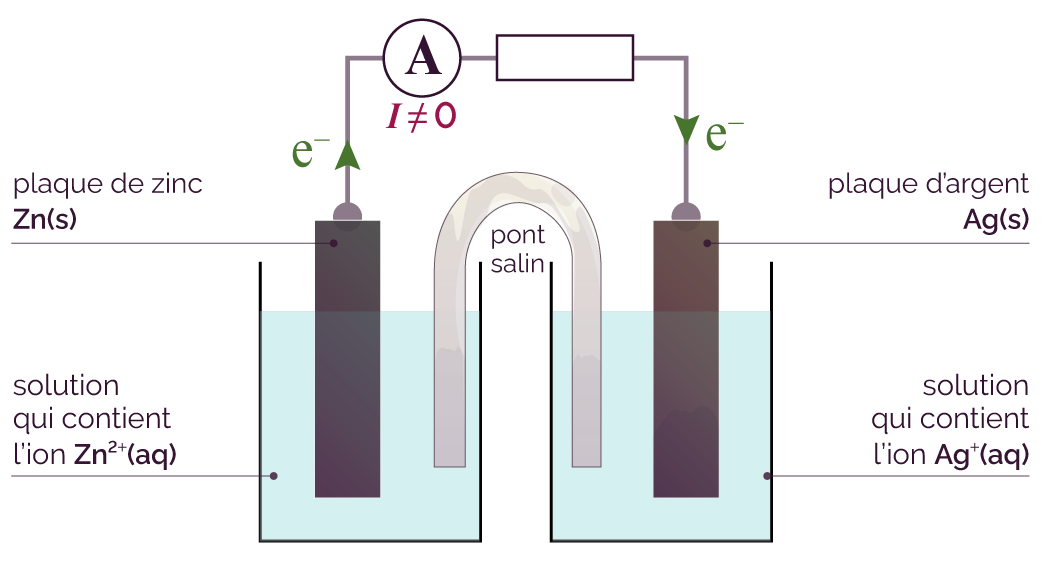
Fonctionnement de la pile zinc-argent
L’intensité mesurée est différente de zéro ampère, ce qui signifie qu’un courant électrique circule entre les deux bornes de la pile.
Le sens de circulation des électrons à l’extérieur de la pile, de l’électrode négative vers l’électrode positive, nous permet de trouver les équations électrochimiques qui ont lieu à chacune des électrodes.
| Électrode | Mouvement des électrons | Équation électrochimique |
| Argent (+) | Les électrons arrivent du circuit sur l’électrode. | Ag+ (aq) + e– → Ag (s) |
| Zinc (–) | Les électrons partent dans le circuit depuis l’électrode. | Zn (s) → Zn2+ (aq) + 2 e– |
L’équation associée au fonctionnement de la pile est donc la suivante.
Zn (s) + 2 Ag+ (aq) → Zn2+ (aq) + 2 Ag (s)

Des quiz et exercices pour mieux assimiler sa leçon
La plateforme de soutien scolaire en ligne myMaxicours propose des quiz et exercices en accompagnement de chaque fiche de cours. Les exercices permettent de vérifier si la leçon est bien comprise ou s’il reste encore des notions à revoir.

Des exercices variés pour ne pas s’ennuyer
Les exercices se déclinent sous toutes leurs formes sur myMaxicours ! Selon la matière et la classe étudiées, retrouvez des dictées, des mots à relier ou encore des phrases à compléter, mais aussi des textes à trous et bien d’autres formats !
Dans les classes de primaire, l’accent est mis sur des exercices illustrés très ludiques pour motiver les plus jeunes.

Des quiz pour une évaluation en direct
Les quiz et exercices permettent d’avoir un retour immédiat sur la bonne compréhension du cours. Une fois toutes les réponses communiquées, le résultat s’affiche à l’écran et permet à l’élève de se situer immédiatement.
myMaxicours offre des solutions efficaces de révision grâce aux fiches de cours et aux exercices associés. L’élève se rassure pour le prochain examen en testant ses connaissances au préalable.

Des vidéos et des podcasts pour apprendre différemment
Certains élèves ont une mémoire visuelle quand d’autres ont plutôt une mémoire auditive. myMaxicours s’adapte à tous les enfants et adolescents pour leur proposer un apprentissage serein et efficace.
Découvrez de nombreuses vidéos et podcasts en complément des fiches de cours et des exercices pour une année scolaire au top !

Des podcasts pour les révisions
La plateforme de soutien scolaire en ligne myMaxicours propose des podcasts de révision pour toutes les classes à examen : troisième, première et terminale.
Les ados peuvent écouter les différents cours afin de mieux les mémoriser en préparation de leurs examens. Des fiches de cours de différentes matières sont disponibles en podcasts ainsi qu’une préparation au grand oral avec de nombreux conseils pratiques.

Des vidéos de cours pour comprendre en image
Des vidéos de cours illustrent les notions principales à retenir et complètent les fiches de cours. De quoi réviser sa prochaine évaluation ou son prochain examen en toute confiance !








