Notion d'énergie interne, interprétation microscopique, variation d'énergie interne
- Fiche de cours
- Quiz et exercices
- Vidéos et podcasts
Insistons sur le fait que ces deux formes d’énergie sont macroscopiques.
• L’énergie cinétique
• Les énergies potentielles concernent notamment l’énergie potentielle de pesanteur
L’énergie totale du système s’écrit comme la somme de l’énergie mécanique et d’une énergie appelée énergie interne notée U :
L’énergie interne rassemble les formes d’énergie microscopiques du système. Elle concerne l’agitation thermique des particules qui composent le système. D’autre part, l’énergie interne inclut des énergies potentielles microscopiques, de différentes natures.
Par la suite, nous allons nous intéresser à donner l’interprétation microscopique de l’énergie interne.
• Pour les solides, l’agitation thermique se traduit par des vibrations des atomes au sein de la matière, c'est-à-dire des mouvements de faible amplitude des atomes. Cette remarque s’applique bien aux cristaux constituant les métaux. Lorsqu’un tel matériau est chauffé, les vibrations sont transmises de proche en proche, ce qui permet d’expliquer microscopiquement la propagation de la chaleur dans les solides (voir fiche dédiée). Une manière imagée de se représenter cela est d’imaginer un ensemble de systèmes masse-ressort.
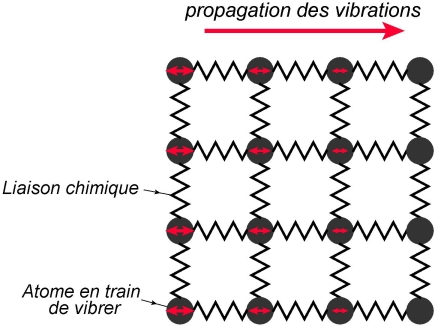
• Pour les liquides, l’agitation thermique se manifeste aussi par des vibrations, mais aussi par un mouvement des molécules les unes par rapport aux autres. Comme vu en 1ère S, cela engendre l’établissement et la rupture continuelle de liaisons basses énergies (liaisons hydrogène ou de Van der Waals) entre les molécules du liquide.
• Pour les gaz, il n’y a pas de liaison intermoléculaire. Pour un gaz monoatomique (gaz rare), l’agitation thermique correspond à l’énergie cinétique des atomes. Ce point sera détaillé au 3. Cette agitation désordonnée est décrite par le modèle du mouvement Brownien, où les seules interactions entre particules sont les collisions qu’elles subissent entre elles. Quand un gaz chaud est mis en contact avec un gaz froid, les collisions assurent une progressive homogénéisation de la température, par un transfert d’énergie cinétique lors des chocs.
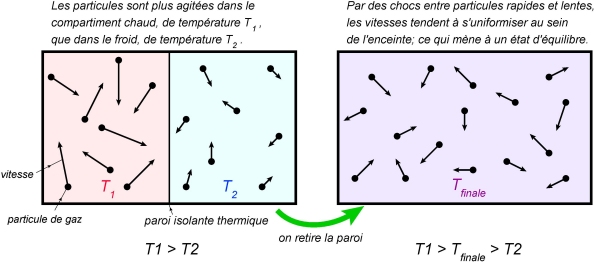
Schématisation de l’agitation thermique dans un gaz
Pour des gaz polyatomiques (diatomiques, etc.), l’agitation thermique se manifeste également via des énergies de vibration et de rotation des molécules.
D’une manière générale, quel que soit l’état physique du système, l’agitation thermique est nommée de la sorte car elle est liée à la notion de température. Autrement dit, la température est une grandeur macroscopique rendant compte de l’agitation interne du système. La température peut être vue comme une grandeur statistique, comme une moyenne.
L’énergie cinétique moyenne
On relie m à la masse molaire M (en kg/mol !), via
Par exemple, la masse molaire moyenne des molécules d’air étant
On peut également citer d’autres formes d’énergies potentielles microscopiques, résultant par exemple de liaisons intermoléculaires. Ces énergies varient lors d’un changement d’état de la matière : fusion, liquéfaction, etc.
La détermination de l’énergie interne pourrait se révéler compliquée (impossible dans la pratique), car il faudrait prendre en compte bon nombre de contributions de natures très diverses. Mais, ce n’est pas l’énergie qui est intéressante dans un calcul, mais sa variation. Ainsi, lorsque le système n’est pas le siège de réactions chimiques ou nucléaires, ce qui sera souvent le cas dans les exemples traités, il n’y aura aucune raison de prendre en compte dans le calcul les énergies associées.
La variation d’énergie interne
Comme
Pour comptabiliser les échanges d’énergies entre le système et son environnement, la convention est qu’une énergie reçue par le système est comptée positivement ; une énergie cédée par le système à son environnement est comptée négativement.
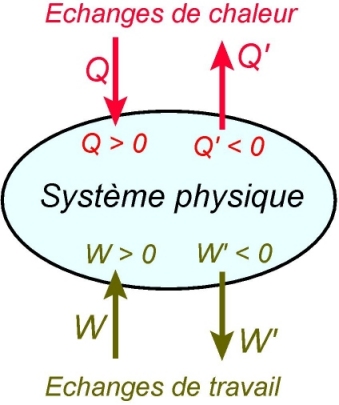
La méthodologie requise pour établir le bilan d’énergie d’un système est détaillé dans une autre fiche (« Bilans d’énergie : transfert thermique et travail »). Il y est également proposé une définition précise des divers systèmes physiques intervenant dans ce type d’études.
Le travail W
Un travail (en J) est une énergie (non thermique) transférée d’un système à un autre, via une « contrainte mécanique ». Ce terme concerne les forces, comme vu l’année dernière. Dans ce cours, on considère les forces qui déforment le système, mais pas celles qui induisent un déplacement de celui-ci (
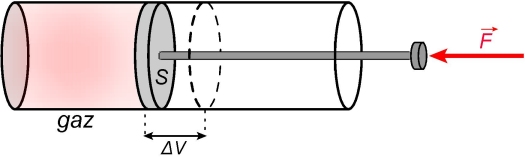
Un opérateur exerce une force
La notion de travail est également élargie à d’autres types de contraintes, par exemple de nature électrique. On pourra alors prendre en compte le travail engendré par un courant électrique, dans un moteur, chauffage électrique, etc.
La quantité de chaleur Q
Q (en J) concerne une énergie apportée ou cédée par le système sous forme de chaleur. Ce transfert peut induire une variation de la température du système, voir fiche « Capacité thermique – variation d’énergie interne par transfert de chaleur ».
• l’agitation thermique du système, associée aux mouvements désordonnés des particules du système. Elle est reliée à la notion macroscopique de température.
• des énergies potentielles microscopiques, comme les énergies chimiques et nucléaires.
Pour un système dont l’énergie mécanique est conservée, son éventuelle variation d’énergie totale

Des quiz et exercices pour mieux assimiler sa leçon
La plateforme de soutien scolaire en ligne myMaxicours propose des quiz et exercices en accompagnement de chaque fiche de cours. Les exercices permettent de vérifier si la leçon est bien comprise ou s’il reste encore des notions à revoir.

Des exercices variés pour ne pas s’ennuyer
Les exercices se déclinent sous toutes leurs formes sur myMaxicours ! Selon la matière et la classe étudiées, retrouvez des dictées, des mots à relier ou encore des phrases à compléter, mais aussi des textes à trous et bien d’autres formats !
Dans les classes de primaire, l’accent est mis sur des exercices illustrés très ludiques pour motiver les plus jeunes.

Des quiz pour une évaluation en direct
Les quiz et exercices permettent d’avoir un retour immédiat sur la bonne compréhension du cours. Une fois toutes les réponses communiquées, le résultat s’affiche à l’écran et permet à l’élève de se situer immédiatement.
myMaxicours offre des solutions efficaces de révision grâce aux fiches de cours et aux exercices associés. L’élève se rassure pour le prochain examen en testant ses connaissances au préalable.

Des vidéos et des podcasts pour apprendre différemment
Certains élèves ont une mémoire visuelle quand d’autres ont plutôt une mémoire auditive. myMaxicours s’adapte à tous les enfants et adolescents pour leur proposer un apprentissage serein et efficace.
Découvrez de nombreuses vidéos et podcasts en complément des fiches de cours et des exercices pour une année scolaire au top !

Des podcasts pour les révisions
La plateforme de soutien scolaire en ligne myMaxicours propose des podcasts de révision pour toutes les classes à examen : troisième, première et terminale.
Les ados peuvent écouter les différents cours afin de mieux les mémoriser en préparation de leurs examens. Des fiches de cours de différentes matières sont disponibles en podcasts ainsi qu’une préparation au grand oral avec de nombreux conseils pratiques.

Des vidéos de cours pour comprendre en image
Des vidéos de cours illustrent les notions principales à retenir et complètent les fiches de cours. De quoi réviser sa prochaine évaluation ou son prochain examen en toute confiance !








