Dissolution d'un solide ionique dans un solvant polaire
- Fiche de cours
- Quiz et exercices
- Vidéos et podcasts
L’eau (
Par contre, des molécules comme les hydrocarbures (ne contenant que des carbones et des hydrogènes) ne sont pas polaires. En effet, elles ne présentent pas de charges partielles, le carbone étant moins électronégatif que l’oxygène. Quelques solvants de ce type sont l’hexane, le cyclohexane, le toluène ou le benzène. On les nomme solvants apolaires.
Ces ions vont être détachés du cristal, car attirés par les molécules d’eau. Ils sont alors désormais libres dans la solution. Ils conserveront des molécules d’eau dans leur environnement proche, ce qui les empêchera de reformer le cristal. Ils ont été solvatés. On parle aussi d’hydratation si le solvant est l’eau.
Le cristal va se dissocier, ce qui correspond macroscopiquement à sa dissolution. La solution s’enrichit en ions ; c’est une solution ionique. Le solide ionique est globalement neutre. Il en est de même pour une solution ionique. Elle va contenir autant de charges positives que de charges négatives. Cela constitue son électroneutralité.
Une dissolution ne se produit pas avec tous les solvants. De manière générale, lorsqu’un solvant n’est pas polaire, la dissolution d’un solide ionique est impossible. En effet, dans l’exemple, on a vu que les molécules d’eau pouvaient solvater les ions du cristal grâce à leur charges partielles. Un solvant apolaire n’aurait rien donné : le sel de cuisine n’est pas soluble dans du cyclohexane par exemple.
NB : (s) pour solide, (aq) pour aqueux.
Lorsque des coefficients interviennent, on a :
Deux lois de conservation seront à respecter : la conservation de la neutralité électrique globale et la conservation des éléments chimiques.
Attention : certains solides ioniques contiennent des molécules d’eau dans leur structure cristalline. Par exemple, le sulfate de cuivre est de couleur bleue car il est pentahydraté : il se note
Pour une d’une espèce chimique X, elle est également notée
La masse m est en gramme, et le volume V en litre. Une concentration massique
Pour passer de la concentration massique à la concentration molaire, il faut déterminer la masse molaire M de l’espèce chimique et employer la relation
La masse m s’exprime en kilogramme, le volume V en litre, et la masse volumique en kg/L. Ce genre de calcul est pertinent pour des solutions concentrées. En effet, dans ce cas, les masses volumiques du solvant et de la solution ne sont pas plus exactement les mêmes.
On appelle solubilité d’un soluté la concentration maximale que l’on peut atteindre avec un solvant donné. La solubilité est exprimée habituellement en g/L. Lorsqu’une solution est saturée, sa concentration massique correspond à la solubilité.
Pour un solvant donné, la solubilité dépend de la température. Pour le chlorure de sodium dissous dans l’eau, elle est de 357 g/L à 0°C, reste stable à 25 °C, puis augmente avec la température. Elle est de 391 g/L à 100 °C.
A température fixée, le choix du solvant influe sur la solubilité d’un soluté. Ainsi, nous avons vu qu’elle est de 357 g/L à 25°C pour le chlorure de sodium dans l’eau, alors qu’elle n’est que de 17,7 g/L pour le même soluté dans le méthanol.
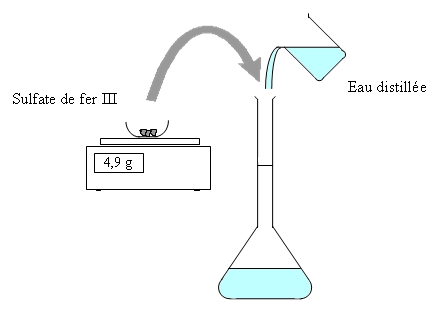
Le sulfate de fer III se dissout selon la réaction
La masse molaire du sulfate de fer III
Il nous faut donc peser une masse
Un solvant polaire a la capacité de dissoudre certains solides ioniques. Les ions qui constituent le cristal passent alors en solution. Ils ont été solvatés. La dissolution d’un solide ionique est traduite par une équation de dissolution, de la forme :
Les solvants non polaires (apolaires) n’ont pas d’action sur les solides ioniques.
Pour mesurer la concentration en soluté dans une solution, on fait appel à la concentration molaire c, en mol/L, par la formule
La solubilité d’un soluté est la concentration maximale que l’on peut atteindre avec un solvant donné. Elle dépend de la température et s’exprime en g/L. Lorsqu’une solution est saturée, il n’est pas possible de dissoudre davantage du soluté. La concentration massique est alors égale à la solubilité.

Des quiz et exercices pour mieux assimiler sa leçon
La plateforme de soutien scolaire en ligne myMaxicours propose des quiz et exercices en accompagnement de chaque fiche de cours. Les exercices permettent de vérifier si la leçon est bien comprise ou s’il reste encore des notions à revoir.

Des exercices variés pour ne pas s’ennuyer
Les exercices se déclinent sous toutes leurs formes sur myMaxicours ! Selon la matière et la classe étudiées, retrouvez des dictées, des mots à relier ou encore des phrases à compléter, mais aussi des textes à trous et bien d’autres formats !
Dans les classes de primaire, l’accent est mis sur des exercices illustrés très ludiques pour motiver les plus jeunes.

Des quiz pour une évaluation en direct
Les quiz et exercices permettent d’avoir un retour immédiat sur la bonne compréhension du cours. Une fois toutes les réponses communiquées, le résultat s’affiche à l’écran et permet à l’élève de se situer immédiatement.
myMaxicours offre des solutions efficaces de révision grâce aux fiches de cours et aux exercices associés. L’élève se rassure pour le prochain examen en testant ses connaissances au préalable.

Des vidéos et des podcasts pour apprendre différemment
Certains élèves ont une mémoire visuelle quand d’autres ont plutôt une mémoire auditive. myMaxicours s’adapte à tous les enfants et adolescents pour leur proposer un apprentissage serein et efficace.
Découvrez de nombreuses vidéos et podcasts en complément des fiches de cours et des exercices pour une année scolaire au top !

Des podcasts pour les révisions
La plateforme de soutien scolaire en ligne myMaxicours propose des podcasts de révision pour toutes les classes à examen : troisième, première et terminale.
Les ados peuvent écouter les différents cours afin de mieux les mémoriser en préparation de leurs examens. Des fiches de cours de différentes matières sont disponibles en podcasts ainsi qu’une préparation au grand oral avec de nombreux conseils pratiques.

Des vidéos de cours pour comprendre en image
Des vidéos de cours illustrent les notions principales à retenir et complètent les fiches de cours. De quoi réviser sa prochaine évaluation ou son prochain examen en toute confiance !








