Comment caractériser les réactifs et les produits ?
- Fiche de cours
- Quiz et exercices
- Vidéos et podcasts
Comment peut-on alors caractériser les produits formés et vérifier que les réactifs ont été consommés ?
Un test caractéristique permet d’identifier sans hésiter une espèce chimique donnée lors d’une analyse chimique.
Lors d’une réaction chimique, on doit
être capable d’identifier les espèces
chimiques introduites initialement pour pouvoir tester si
elles sont encore présentes en fin de
réaction. Deux hypothèses devront alors
être étudiées :
- soit l’espèce chimique n’a pas
réagi ;
- soit elle a été introduite en
excès.
En ce qui concerne les produits, le chimiste ne doit pas nécessairement réaliser tous les tests qu’il connaît. Il doit pouvoir faire des hypothèses à partir des réactifs mis en jeu. En effet, une réaction chimique n’est en fait qu’une réorganisation de la matière : « Rien ne se perd, rien ne se crée, tout se transforme » ! (Lavoisier).
• Test des ions chlorure : les ions chlorure Cl- sont testés au nitrate d’argent. Un précipité blanc de chlorure d’argent qui noircit à la lumière apparaît selon l’équation : Ag+(aq) + Cl-(aq) → AgCl(s).
• Test des cations métalliques : les ions métalliques comme Fe3+ (ferrique) ; Fe2+ (ferreux) ; Al3+ (Aluminium) ; Zn2+ (zinc) ; Cu2+ (cuivre) se testent à la soude ou hydroxyde de sodium Na+(aq) + HO-(aq). On obtient alors un précipité caractéristique :
|
Fe3+(aq) + HO-(aq) → Fe(OH)3 (s) |
précipité orange |
|
Fe2+(aq) + HO-(aq) → Fe(OH)2 (s) |
précipité vert |
|
Al3+(aq) + HO-(aq) → Al(OH)3 (s) |
précipité blanc qui |
|
Zn2+(aq) + HO-(aq) → Zn(OH)2 (s) |
précipité blanc |
|
Cu2+(aq) + HO-(aq) → Cu(OH)2 (s) |
précipité bleu |
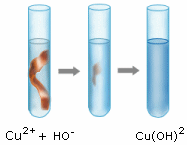
Test caractéristique des ions
Cu2+
• Présence d’ions hydrogène : La présence d’ions hydrogène peut être montrée avec du papier pH car un acide libère des ions H+ et possède un pH<7.
Le test de l’eau est connu depuis le collège. En effet, le sulfate de cuivre anhydre est une poudre blanche alors que le sulfate de cuivre hydraté est bleu. Au contact de l’eau, le sulfate de cuivre anhydre se colore donc en bleu !
A ce niveau, on doit au moins connaître trois gaz
et pouvoir les identifier :
• Le
dioxygène O2
ravive une bûchette incandescente (c’est un
comburant).
• Le dihydrogène
H2 crée une
détonation en présence d’une
allumette (mélange tonnant avec
le dioxygène de l’air).
• Le dioxyde de carbone
CO2 se teste à
l’eau de chaux où un
précipité blanc apparaît.
Dans l’exemple choisi de l’énoncé (pluie acide sur une toiture en zinc) ; si on réalise une simulation de l’expérience, on peut identifier dans l’état initial de la transformation chimique :
• la solution au départ est acide (morceau de papier pH).
Dans l’état final, le morceau de zinc a disparu mais :
• la solution est acide (test au papier pH), donc l’acide a été introduit en excès,
• les ions chlorure sont toujours présents (test au nitrate d’argent positif),
• un gaz s’est dégagé : c’est du dihydrogène (test à l’allumette : détonation).
Réactifs et produits peuvent être mis en évidence par des tests caractéristiques afin de pouvoir décrire sans hésiter l’état initial et l’état final de la transformation chimique étudiée.

Des quiz et exercices pour mieux assimiler sa leçon
La plateforme de soutien scolaire en ligne myMaxicours propose des quiz et exercices en accompagnement de chaque fiche de cours. Les exercices permettent de vérifier si la leçon est bien comprise ou s’il reste encore des notions à revoir.

Des exercices variés pour ne pas s’ennuyer
Les exercices se déclinent sous toutes leurs formes sur myMaxicours ! Selon la matière et la classe étudiées, retrouvez des dictées, des mots à relier ou encore des phrases à compléter, mais aussi des textes à trous et bien d’autres formats !
Dans les classes de primaire, l’accent est mis sur des exercices illustrés très ludiques pour motiver les plus jeunes.

Des quiz pour une évaluation en direct
Les quiz et exercices permettent d’avoir un retour immédiat sur la bonne compréhension du cours. Une fois toutes les réponses communiquées, le résultat s’affiche à l’écran et permet à l’élève de se situer immédiatement.
myMaxicours offre des solutions efficaces de révision grâce aux fiches de cours et aux exercices associés. L’élève se rassure pour le prochain examen en testant ses connaissances au préalable.

Des vidéos et des podcasts pour apprendre différemment
Certains élèves ont une mémoire visuelle quand d’autres ont plutôt une mémoire auditive. myMaxicours s’adapte à tous les enfants et adolescents pour leur proposer un apprentissage serein et efficace.
Découvrez de nombreuses vidéos et podcasts en complément des fiches de cours et des exercices pour une année scolaire au top !

Des podcasts pour les révisions
La plateforme de soutien scolaire en ligne myMaxicours propose des podcasts de révision pour toutes les classes à examen : troisième, première et terminale.
Les ados peuvent écouter les différents cours afin de mieux les mémoriser en préparation de leurs examens. Des fiches de cours de différentes matières sont disponibles en podcasts ainsi qu’une préparation au grand oral avec de nombreux conseils pratiques.

Des vidéos de cours pour comprendre en image
Des vidéos de cours illustrent les notions principales à retenir et complètent les fiches de cours. De quoi réviser sa prochaine évaluation ou son prochain examen en toute confiance !








