Comment calculer une masse molaire moléculaire ?
- Fiche de cours
-
Quiz et exercices
1
- Vidéos et podcasts
Une mole d'atomes de carbone
Une telle quantité d'atomes a une certaine masse appelée masse molaire atomique.
On la note M et son unité est le gramme par mole (g·moI-1).
Le bore à l'état naturel est constitué d'un mélange de bore 10B à hauteur de 19,64 % et de bore 11B à hauteur de 80,36 %.
Ainsi, la masse molaire du bore s'écrit :
Soit :
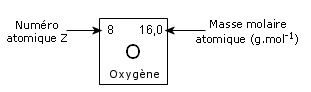
Dans le classement périodique actuel, on trouve facilement la masse molaire atomique d'un élément :
La masse d'une molécule d'eau est donc la masse de 2 atomes d'hydrogène plus un atome d'oxygène. Une mole de molécule d'eau est constituée de 6,02.1023 molécules d'eau.
La masse d'une mole d'eau est donc la masse molaire de l'oxygène et 2 fois la masse molaire de l'hydrogène soit :
M(H2O) = 2M(H) + M(O) soit M(H2O) = 2 × 1,0 + 16,0 = 18 g·mol-1.
La masse molaire moléculaire correspond donc à la somme des coefficients des masses molaires atomiques des atomes qui la constituent. Comme la masse molaire atomique, son unité est le gramme par mole (g·mol-1).
Teste dès maintenant tes nouvelles connaissances dans notre quiz
Vous avez obtenu75%de bonnes réponses !
Reçois l’intégralité des bonnes réponses ainsi que les rappels de cours associés

Des vidéos et des podcasts pour apprendre différemment
Certains élèves ont une mémoire visuelle quand d’autres ont plutôt une mémoire auditive. myMaxicours s’adapte à tous les enfants et adolescents pour leur proposer un apprentissage serein et efficace.
Découvrez de nombreuses vidéos et podcasts en complément des fiches de cours et des exercices pour une année scolaire au top !

Des podcasts pour les révisions
La plateforme de soutien scolaire en ligne myMaxicours propose des podcasts de révision pour toutes les classes à examen : troisième, première et terminale.
Les ados peuvent écouter les différents cours afin de mieux les mémoriser en préparation de leurs examens. Des fiches de cours de différentes matières sont disponibles en podcasts ainsi qu’une préparation au grand oral avec de nombreux conseils pratiques.

Des vidéos de cours pour comprendre en image
Des vidéos de cours illustrent les notions principales à retenir et complètent les fiches de cours. De quoi réviser sa prochaine évaluation ou son prochain examen en toute confiance !








