Utiliser la loi de Coulomb
- Fiche de cours
- Quiz et exercices
- Vidéos et podcasts
- Connaitre la loi de Coulomb.
- Faire le lien entre les signes des charges électriques des corps et la force répulsive/attractive.
- Connaitre l’interaction électrostatique et faire le lien avec la loi de Coulomb.
- Comprendre la cohésion d’un cristal ionique en comparant les valeurs des forces électrostatiques entre cations et anions au sein du cristal, en utilisant la loi de Coulomb.
- Un corps qui porte une charge électrique exerce une force électrostatique sur un autre corps chargé.
- Si les charges sont de même signe, la force électrostatique est répulsive et si les charges électriques sont de signes opposés, la force électrostatique est attractive.
- L’intensité de la force électrostatique est donnée par la loi de Coulomb, en newton.
- Comparer deux forces électrostatiques consiste à calculer le rapport (division) entre les deux valeurs des intensités.
- Dans un cristal ionique, la force attractive entre un cation et un anion est supérieure à celle répulsive entre deux cations ou entre deux anions. C’est ce qui explique la cohésion du cristal ionique.
- Loi de Coulomb
- Force
- Charge d’un électron
On considère deux corps ponctuels notés A et B, qui portent respectivement des charges électriques notées qA et qB. La distance entre ces deux corps est égale à dAB.
Le corps A exerce sur le corps B une force
électrostatique qui est modélisée
par un vecteur force ![]() .
.
La force peut être attractive ou répulsive, en fonction des signes respectifs des deux charges.
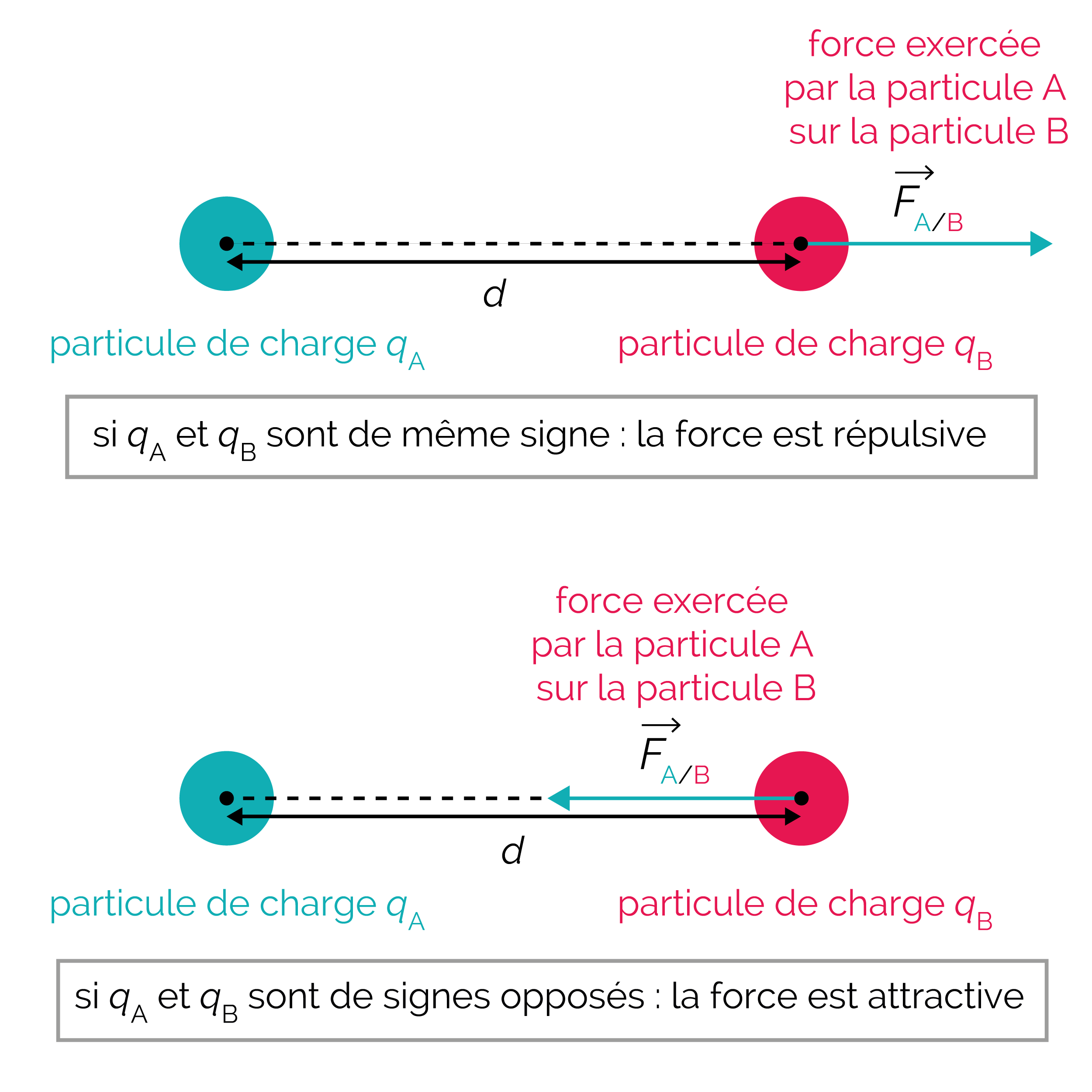
Force répulsive ou attractive en fonction du signe des charges
L’intensité de la force est
notée ![]() et s’exprime en newton
(N) : elle est donnée par la loi de Coulomb.
et s’exprime en newton
(N) : elle est donnée par la loi de Coulomb.
|
|
avec :
|
La double barre signifie qu’il s’agit d’une valeur absolue. En mathématiques, la valeur absolue d’un nombre correspond à sa valeur sans tenir compte de son signe.
On calcule l’intensité de la force électrostatique exercée par une particule de charge électrique qA = 4,8 × 10–19 C sur un électron de charge électrique qB = –1,6 × 10–19 C.
Les deux particules sont distantes l’une de l’autre de d = 5,0 × 10–8 m.
On applique la loi de Coulomb :
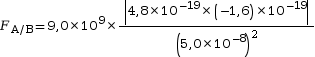
La charge électrique portée par un électron est égale à –1,6 × 10–19 C et est notée –e, où e est la charge électrique élémentaire (e = 1,6 × 10–19 C). Cette charge électrique élémentaire permet de calculer la charge portée par un ion.
| Formule de l’ion | Nombre de charges élémentaires portées | Calcul de la charge de l’ion |
| O2– | 2 négatives | 2 × (–1,6 × 10–19) = –3,2 × 10–19 C |
| Al3+ | 3 positives | 3 × 1,6 × 10–19 = 4,8 × 10–19 C |
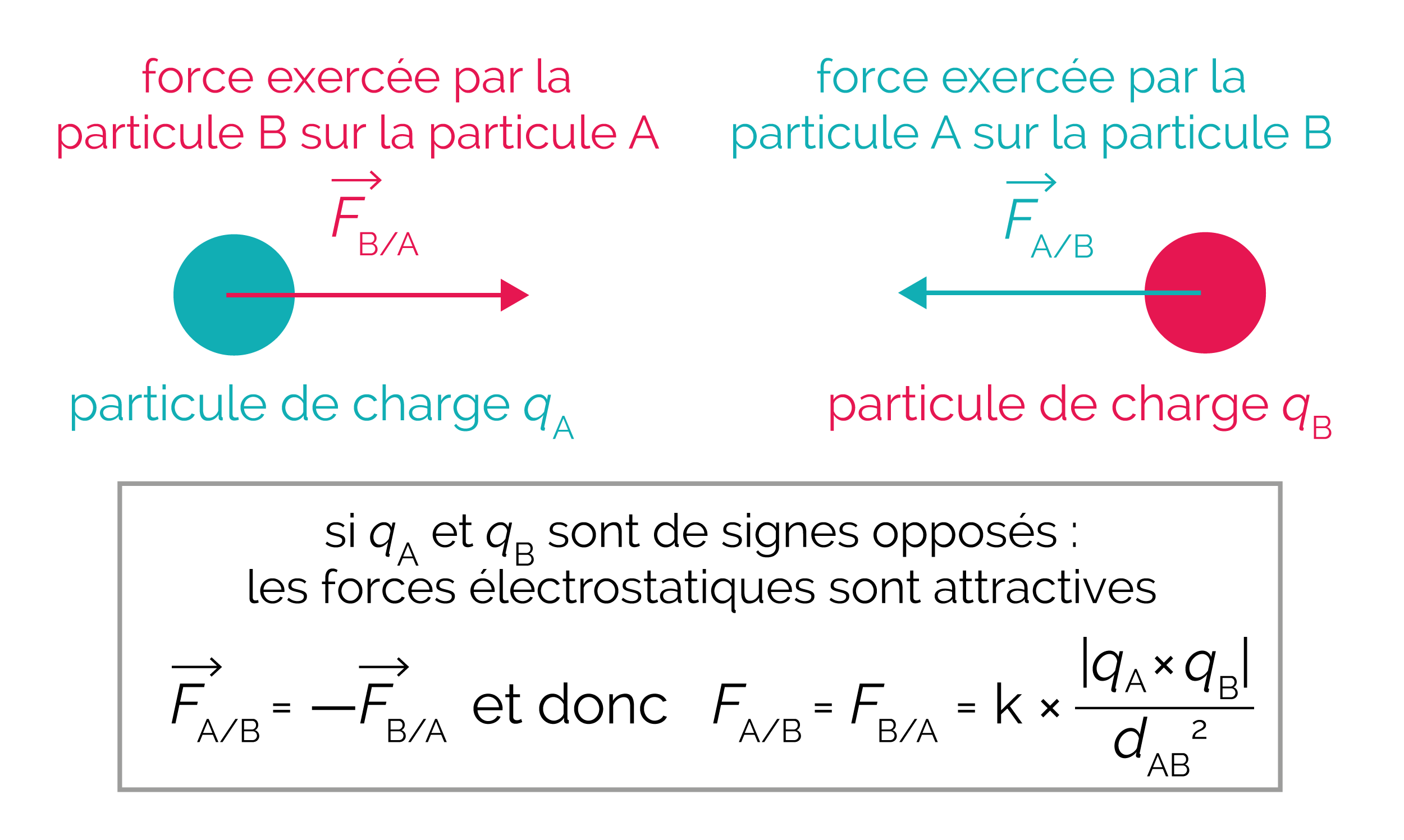
Deux corps chargés exercent l’un sur l’autre des forces électrostatiques qui peuvent être répulsives ou attractives, en fonction des signes de leurs charges.

Un cristal ionique est un solide composé d’un type de cation et d’un type d’anion, qui sont régulièrement disposés dans l’espace.
Le chlorure de sodium de formule NaCl(s) est composé du cation sodium Na+ et de l’anion chlorure Cl–.

Cristal ionique de chlorure de sodium
Les ions chlorure exercent entre eux une interaction électrostatique répulsive, tout comme les ions sodium entre eux. L’interaction électrostatique entre un ion sodium et un ion chlorure est attractive.
Les distances moyennes entre les différentes entités chimiques sont données ci–dessous.
| Distance entre | Cl– et Cl– | Na+ et Na+ | Na+ et Cl– |
| d (en m) | 3,93 × 10–10 | 3,93 × 10–10 | 2,78 × 10–10 |
L’ion chlorure Cl– porte une charge négative élémentaire q = –1,60 × 10–19 C et l’ion sodium porte une charge positive élémentaire q = 1,60 × 10–19 C.
On calcule l’intensité des forces électrostatiques en appliquant la loi de Coulomb.
| Ions étudiés | Cl– et Cl– | Na+ et Na+ | Na+ et Cl– |
| Force électrostatique F (en N) |
1,5 × 10–9 (force répulsive) |
1,5 × 10–9 (force répulsive) |
3,0 × 10–9 (force attractive) |
On compare la force répulsive entre les anions ou entre les cations, à celle attractive entre cation et anion :
![]()
La force électrostatique attractive est donc deux fois plus grande que la force répulsive.
On peut donc conclure que la force électrostatique attractive entre un cation sodium et un anion chlorure est responsable de la cohésion du cristal ionique de chlorure de sodium.

Des quiz et exercices pour mieux assimiler sa leçon
La plateforme de soutien scolaire en ligne myMaxicours propose des quiz et exercices en accompagnement de chaque fiche de cours. Les exercices permettent de vérifier si la leçon est bien comprise ou s’il reste encore des notions à revoir.

Des exercices variés pour ne pas s’ennuyer
Les exercices se déclinent sous toutes leurs formes sur myMaxicours ! Selon la matière et la classe étudiées, retrouvez des dictées, des mots à relier ou encore des phrases à compléter, mais aussi des textes à trous et bien d’autres formats !
Dans les classes de primaire, l’accent est mis sur des exercices illustrés très ludiques pour motiver les plus jeunes.

Des quiz pour une évaluation en direct
Les quiz et exercices permettent d’avoir un retour immédiat sur la bonne compréhension du cours. Une fois toutes les réponses communiquées, le résultat s’affiche à l’écran et permet à l’élève de se situer immédiatement.
myMaxicours offre des solutions efficaces de révision grâce aux fiches de cours et aux exercices associés. L’élève se rassure pour le prochain examen en testant ses connaissances au préalable.

Des vidéos et des podcasts pour apprendre différemment
Certains élèves ont une mémoire visuelle quand d’autres ont plutôt une mémoire auditive. myMaxicours s’adapte à tous les enfants et adolescents pour leur proposer un apprentissage serein et efficace.
Découvrez de nombreuses vidéos et podcasts en complément des fiches de cours et des exercices pour une année scolaire au top !

Des podcasts pour les révisions
La plateforme de soutien scolaire en ligne myMaxicours propose des podcasts de révision pour toutes les classes à examen : troisième, première et terminale.
Les ados peuvent écouter les différents cours afin de mieux les mémoriser en préparation de leurs examens. Des fiches de cours de différentes matières sont disponibles en podcasts ainsi qu’une préparation au grand oral avec de nombreux conseils pratiques.

Des vidéos de cours pour comprendre en image
Des vidéos de cours illustrent les notions principales à retenir et complètent les fiches de cours. De quoi réviser sa prochaine évaluation ou son prochain examen en toute confiance !








