Soigner par thérapie génique
- Fiche de cours
- Quiz et exercices
- Vidéos et podcasts
- Définir la notion de thérapie génique.
- Comprendre le principe de transgénèse ex vivo.
- Comprendre le rôle du vecteur viral en thérapie génique.
- Comprendre le principe du CRISPR-ARN pour la réparation des séquences ADN.
- Comprendre le principe du « saut d’exon ».
- Comprendre le principe de l’immunothérapie.
- Comprendre le mode d’action des ARN antisens.
- Aujourd’hui la médecine fait face à de nombreuses pathologies que le développement des biotechnologies permet d’envisager de soigner.
- Dans ce contexte, la thérapie génique qui consiste à modifier/réparer les gènes impliqués dans les maladies génétiques ouvrent de nouvelles perspectives. En effet, il est possible d’introduire un gène sain dans une cellule pour remplacer le gène malade, mais aussi de réparer directement le gène altéré dans le génome de la cellule.
- La thérapie génique, couplée à la thérapie cellulaire, permet de développer de nouvelles stratégies de lutte contre le cancer. En effet, il est possible de modifier les propriétés de certaines cellules, comme les lymphocytes T, afin qu’elles soient spécifiques des cellules tumorales et les détruisent.
- D’autres molécules, comme les ARN antisens, permettent de bloquer l’expression des oncogènes.
- Toutes ces approches thérapeutiques sont testées dans les cellules in vitro ou chez l’animal. Certaines en sont aujourd’hui au stade d’essai clinique chez l’Homme.
- Le cycle cellulaire
- Mutations de l’ADN et variabilité génétique
- L’expression du patrimoine génétique
- La réponse immunitaire à médiation humorale
- La réponse immunitaire à médiation cellulaire
La thérapie génique a tout d’abord été envisagée pour le traitement des maladies monogéniques. En effet, même si le diagnostic peut être posé précocement pour patients concernés, seuls des approches thérapeutiques visant à atténuer les symptômes peuvent leur être proposées, mais elles ne permettent malheureusement pas la guérison. Le recours à ces thérapies permet tout au plus l’augmentation de l’espérance de vie, seulement dans certains cas.
La thérapie génique avait donc pour ambition initiale de corriger le gène défectueux dans les cellules du malade, afin de permettre la production de la protéine normale.
Aujourd’hui, la thérapie génique peut être envisagée dans d’autres pathologies, telles que les cancers.
Le gène sain (ou gène d’intérêt) est transféré dans le génome de la cellule et se rajoute à son patrimoine génétique par le biais d’un vecteur, le plus souvent d’origine virale. Ce dernier consiste en un virus rendu inoffensif dans lequel le gène d’intérêt a été inséré. On utilise ensuite ses capacités à infecter une cellule pour permettre le transfert du gène d’intérêt dans la cellule cible. Suivant le vecteur utilisé, le gène d’intérêt peut ou non s’intégrer dans le génome de la cellule cible. Si c’est le cas, il pourra être transmis aux cellules filles lors de la mitose.
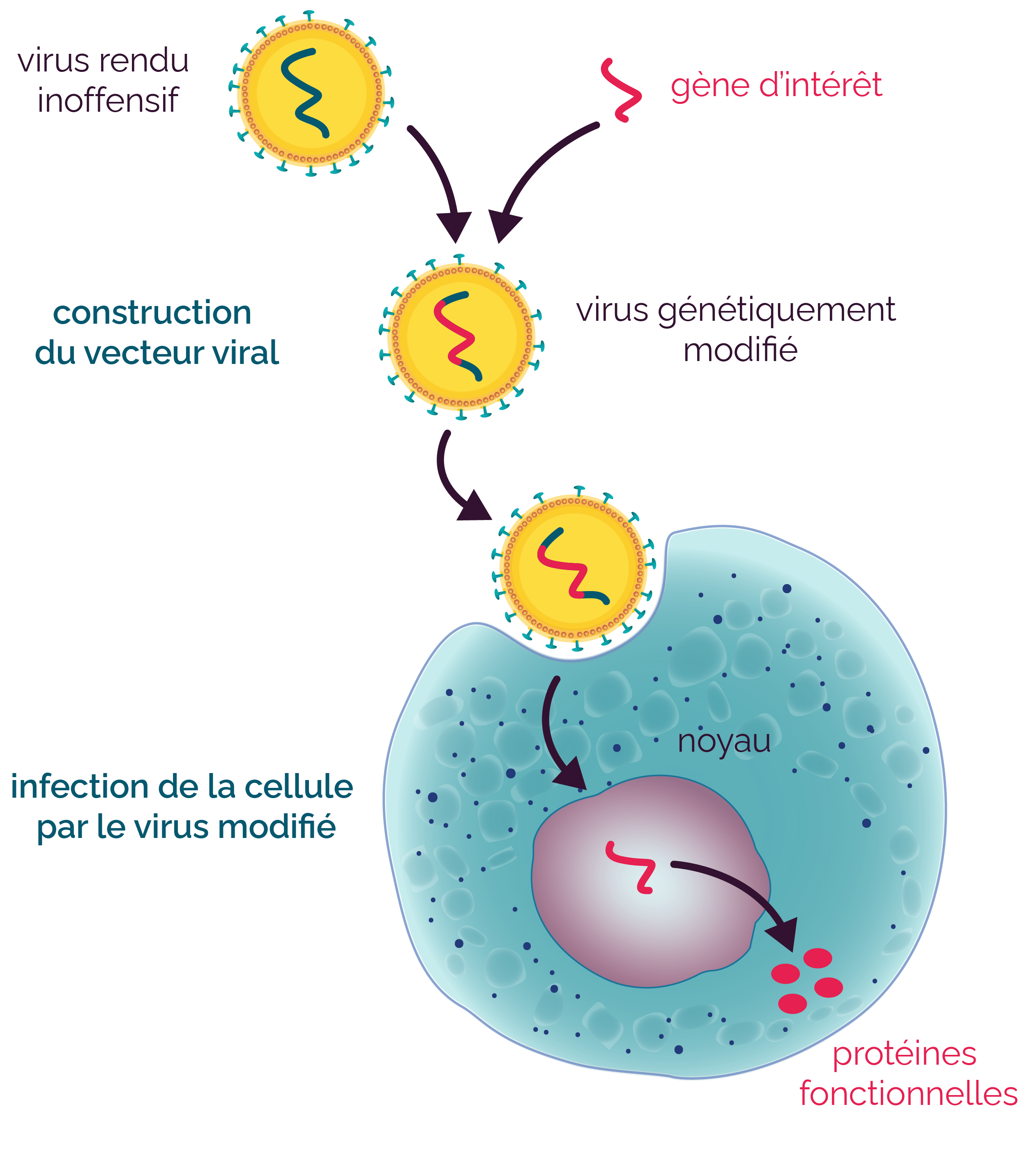
Deux stratégies de transfert du gène sain sont possibles : in vivo et ex vivo.
1. In vivo
Le gène est transféré par injection dans l’organisme ou l’organe à cibler afin qu’il s’intègre dans le génome des cellules non fonctionnelles.
2. Ex vivo
Des cellules souches sont
prélevées dans l’organisme à
traiter. Dans ce cas, le transfert du gène
d’intérêt, ou
transgénèse, se fait
directement dans la cellule. La cellule
« corrigée » sera ensuite
réinjectée puis se
différenciera pour donner une nouvelle cellule
spécialisée fonctionnelle.
Cette seconde approche est notamment utilisée
dans le cas de maladies touchant les cellules
sanguines.
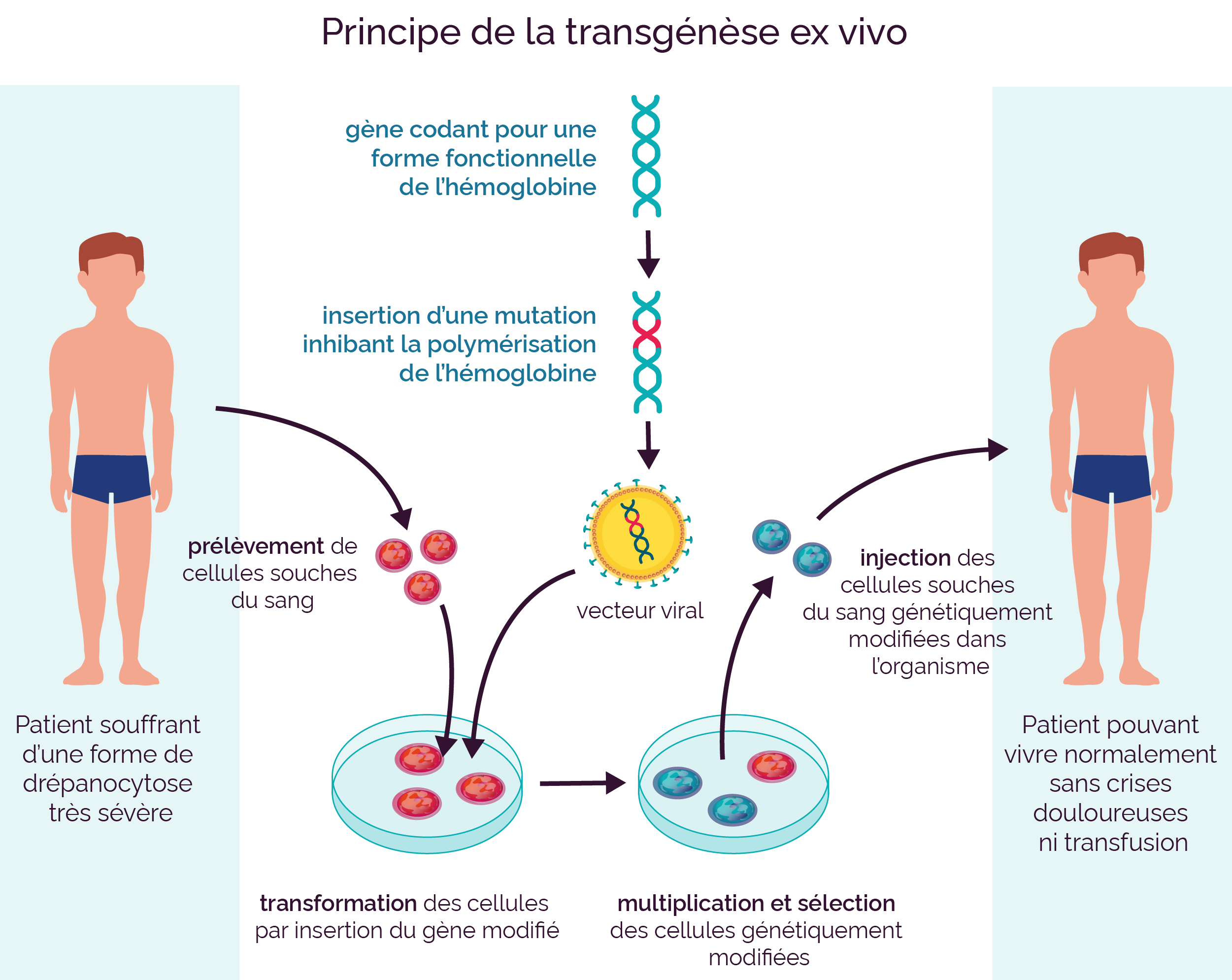
Les avancées en biotechnologie ont permis de mieux connaître la nature des mutations à l’origine des maladies génétiques. Il est donc envisageable de cibler les séquences ADN mutées afin de les réparer directement dans le génome de la cellule défectueuse sans en modifier le patrimoine génétique.
Pour cela, les scientifiques utilisent des ciseaux moléculaires. Ce sont des enzymes particulières, des nucléases, capables de découper l’ADN en reconnaissant spécifiquement des séquences restreintes.
Pour cibler la séquence à découper, l’enzyme est couplée à un fragment d’ARN dont la séquence, complémentaire de l’allèle défectueux à corriger, va permettre la reconnaissance de celui-ci. Une fois que la nucléase a découpé la portion d’ADN portant la mutation, le fragment d’ADN réparé peut être intégré à sa place.
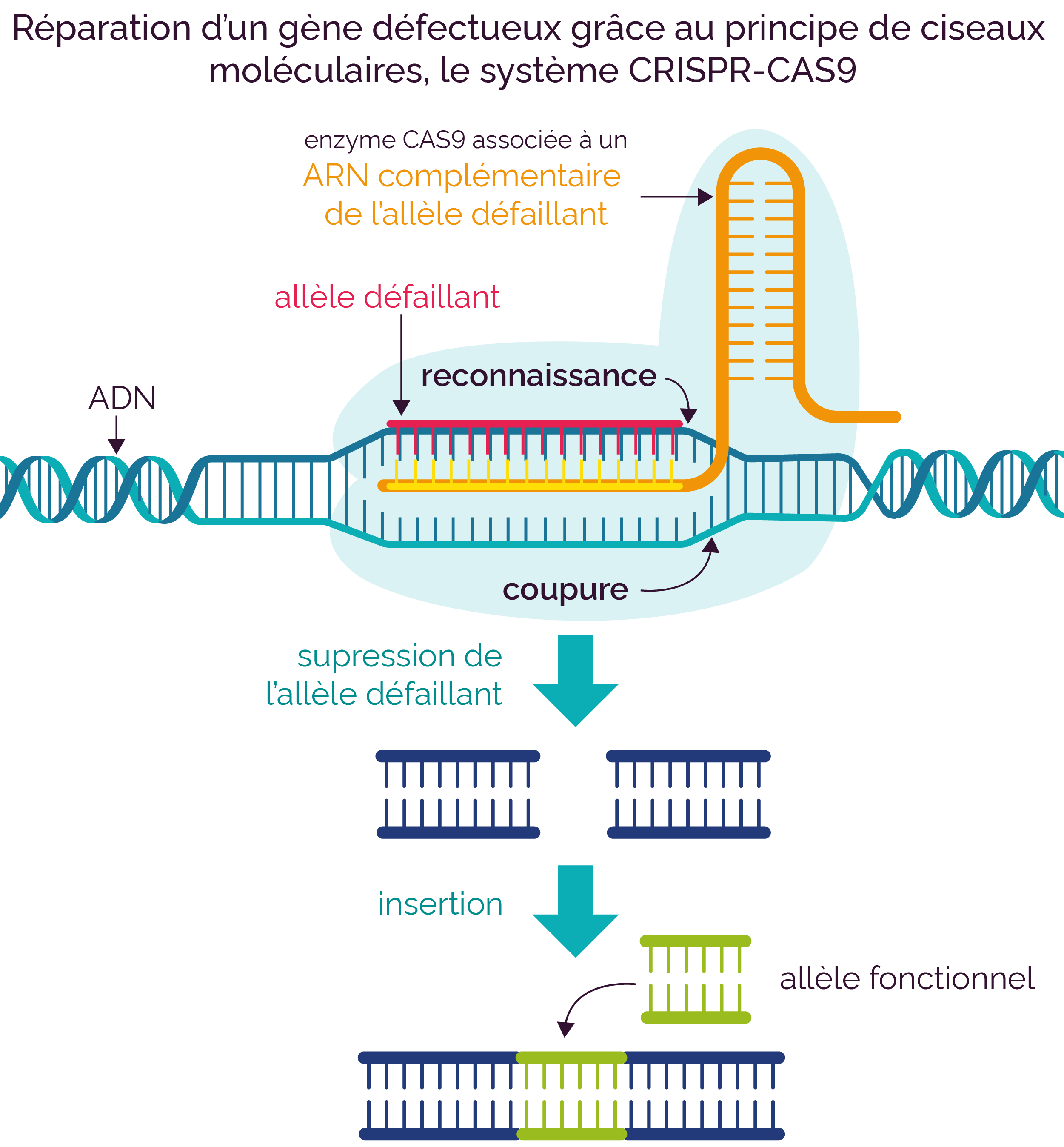
Cette approche, très prometteuse pour le traitement de plusieurs maladies génétiques, reste pour l’instant au stade expérimental.
Dans le cas d’une maladie génétique, c’est une protéine défectueuse qui est en cause. Il est envisageable de corriger soit la séquence du gène codant cette protéine, soit la séquence des ARNm qui servent de matrice pour la traduction. Cette approche a été expérimentée pour traiter la myopathie de Duchenne. Chez les patients atteints par cette maladie, le gène DMD, qui code la dystrophine, présente une mutation localisée sur un des exons, conservé lors de l’épissage de l’ARN prémessager.
Des scientifiques ont utilisé un vecteur viral, contenant des ciseaux moléculaires spécifiques (de type CRISPR), et des fragments d’ARNs, permettant de cibler les séquences situées de part et d’autre de l’exon à exciser.
Le vecteur a été injecté dans les cellules musculaires d’une souris porteuse de la mutation. Les ciseaux moléculaires, en combinaison avec les fragments d’ARNs, ont permis l’excision de l’exon muté. La protéine formée est alors tronquée mais reste partiellement fonctionnelle.
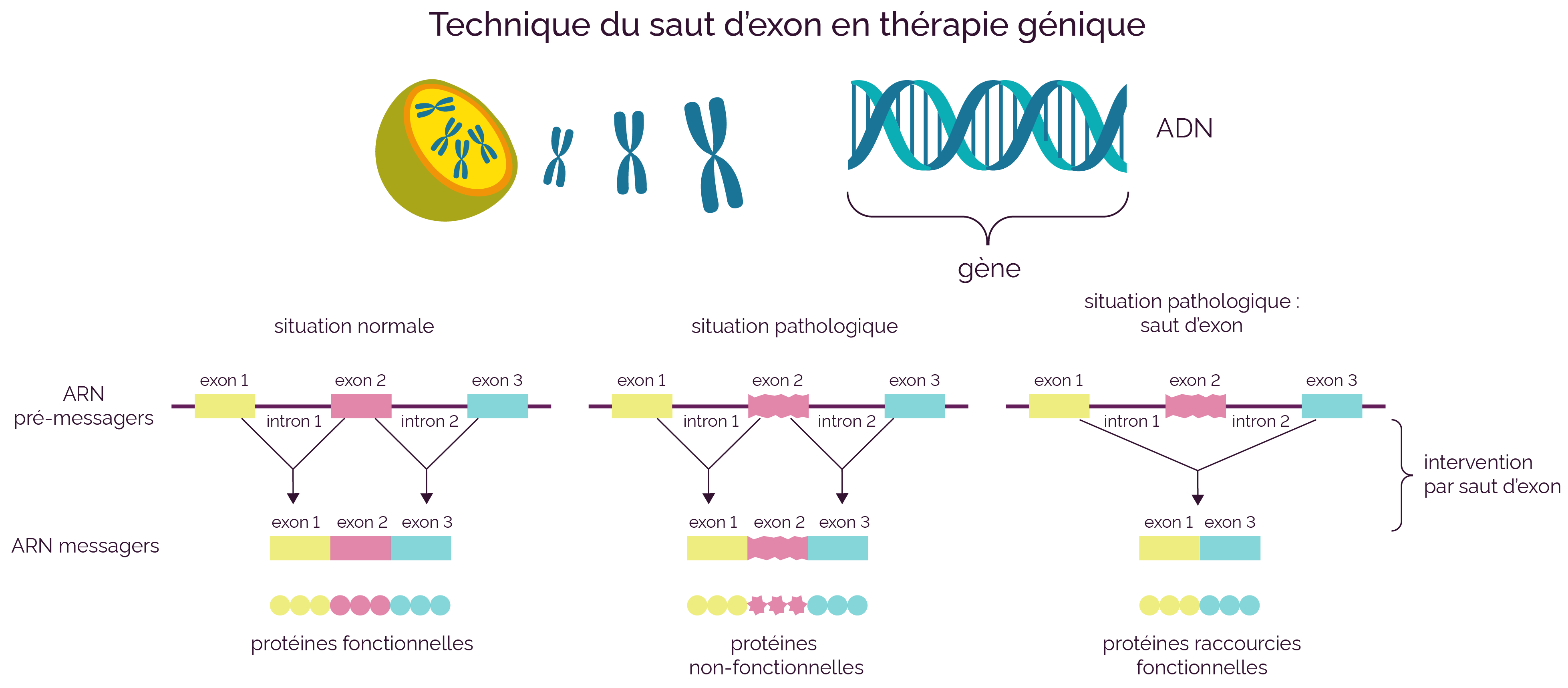
Les cellules cancéreuses sont des cellules qui se multiplient de façon anarchique au sein d’un tissu. Ces cellules présentent à leur surface des antigènes anormaux, qui font d’elles des cibles potentielles du système immunitaire du malade.
Il est possible d’isoler du sang du patient des lymphocytes T et de les modifier génétiquement. Cette modification leur permet d’exprimer à leur surface des récepteurs T capables de reconnaître des antigènes tumoraux. Une fois réinjectés au patient, ces lymphocytes T pourront reconnaître et détruire spécifiquement les cellules cancéreuses. On parle d’immunothérapie.
Les cellules CAR T, utilisées dans le traitement de certaines leucémies B, sont capables de reconnaître l’antigène CD19, présent uniquement à la surface des cellules tumorales.
Une approche consiste à utiliser des molécules d’ARN antisens dont la séquence est complémentaire des ARNm ciblés. Une fois présents dans la cellule, ces ARN antisens s’associent aux ARNm, bloquant ainsi l’expression de la protéine. Il est donc envisageable de recourir à ce mécanisme afin de bloquer l’expression des gènes codant pour les protéines favorisant le développement des tumeurs. Ces gènes sont nommés oncogènes.

Des quiz et exercices pour mieux assimiler sa leçon
La plateforme de soutien scolaire en ligne myMaxicours propose des quiz et exercices en accompagnement de chaque fiche de cours. Les exercices permettent de vérifier si la leçon est bien comprise ou s’il reste encore des notions à revoir.

Des exercices variés pour ne pas s’ennuyer
Les exercices se déclinent sous toutes leurs formes sur myMaxicours ! Selon la matière et la classe étudiées, retrouvez des dictées, des mots à relier ou encore des phrases à compléter, mais aussi des textes à trous et bien d’autres formats !
Dans les classes de primaire, l’accent est mis sur des exercices illustrés très ludiques pour motiver les plus jeunes.

Des quiz pour une évaluation en direct
Les quiz et exercices permettent d’avoir un retour immédiat sur la bonne compréhension du cours. Une fois toutes les réponses communiquées, le résultat s’affiche à l’écran et permet à l’élève de se situer immédiatement.
myMaxicours offre des solutions efficaces de révision grâce aux fiches de cours et aux exercices associés. L’élève se rassure pour le prochain examen en testant ses connaissances au préalable.

Des vidéos et des podcasts pour apprendre différemment
Certains élèves ont une mémoire visuelle quand d’autres ont plutôt une mémoire auditive. myMaxicours s’adapte à tous les enfants et adolescents pour leur proposer un apprentissage serein et efficace.
Découvrez de nombreuses vidéos et podcasts en complément des fiches de cours et des exercices pour une année scolaire au top !

Des podcasts pour les révisions
La plateforme de soutien scolaire en ligne myMaxicours propose des podcasts de révision pour toutes les classes à examen : troisième, première et terminale.
Les ados peuvent écouter les différents cours afin de mieux les mémoriser en préparation de leurs examens. Des fiches de cours de différentes matières sont disponibles en podcasts ainsi qu’une préparation au grand oral avec de nombreux conseils pratiques.

Des vidéos de cours pour comprendre en image
Des vidéos de cours illustrent les notions principales à retenir et complètent les fiches de cours. De quoi réviser sa prochaine évaluation ou son prochain examen en toute confiance !









