Synthèse et hémisynthèse de molécules biologiquement actives
- Fiche de cours
- Quiz et exercices
- Vidéos et podcasts
• Les quantités de substances actives sont en très petites quantités dans les plantes. A l’échelle d’une population, cela demanderait des quantités énormes de plantes.
• La synthèse est moins chère.
• Les molécules actives sont souvent mélangées dans les plantes à d’autres substances non souhaitées, et la séparation n’est pas aisée.
• Certaines molécules naturelles présentent des effets secondaires.
Une synthèse chimique consiste à fabriquer une nouvelle molécule à partir d’une ou plusieurs réactions chimiques. L’enjeu d’une synthèse est de partir de molécules faciles à se procurer (peu chères), en ayant un rendement le plus élevé possible, ce qui inclut l’énergie investie (chauffage). Il faut aussi tenir compte de l’éventuelle nocivité/toxicité de certains réactifs, produits intermédiaires ou sous produits de réaction. Enfin, il est nécessaire de prévoir l’extraction et la purification de la molécule à synthétiser.
Une hémisynthèse est un cas particulier de synthèse chimique. La molécule de départ est issue directement de substances naturelles et correspond quasiment dans sa structure à la molécule que l’on souhaite produire. L’enjeu d’une hémisynthèse est une légère modification afin de faire acquérir à la molécule cible des propriétés qu’elle n’avait pas, ou la rendre plus assimilable pour un consommateur. L’intérêt par rapport à une synthèse est d’économiser des étapes dans la fabrication.
| Nom | Structure | Remarque |
| Alcool |
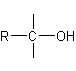
|
Le carbone porteur du groupe hydroxyle OH doit être tétragonal : 4 liaisons simples. |
| Éther |
|
|
| Aldéhyde |
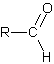
|
Fonction en bout de chaîne carbonée. |
| Cétone |
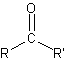
|
|
| Acide carboxylique |
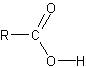
|
Caractère acide de la molécule. |
| Ester |
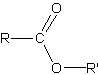
|
Molécule pouvant présenter des propriétés odorantes : parfums. |
| Amine primaire |
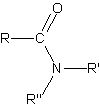
|
Caractère basique de la molécule. |
| Amide |

|
Souvent, R’ ou R’’ se
résument à un atome
d’hydrogène. En SVT, les liaisons peptidiques sont des amides. |
| Phénol |
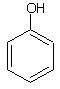
|
Groupe hydroxyle porté par un cycle benzénique. N’est pas un alcool, ou alors un « alcool particulier ». |
| Anhydride d'acide |
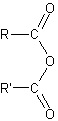
|
Obtenu par déshydratation d’acide carboxylique. Très réactifs. |
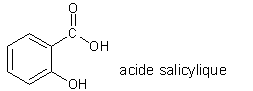
Cependant, par hémisynthèse à partir de l’acide salicylique, on produit l’acide acétylsalicylique, plus connu sous le nom d’aspirine. En effet, celle-ci est plus performante comme médicament, a des propriétés anti-inflammatoires, et est moins nocive pour l’estomac. Elle conserve les propriétés de l’acide salicylique, sauf l’effet antiseptique. L’aspirine peut être produite par réaction de l’acide salicylique avec l’acide éthanoïque, appelé aussi acide acétique :
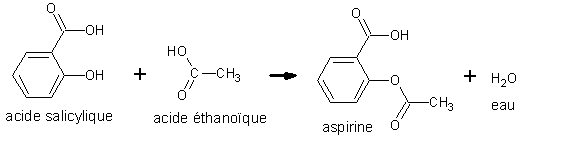
Toutefois, le rendement de cette réaction est limité à 8%. Afin de l’augmenter, on a la possibilité de remplacer l’acide éthanoïque par de l’anhydride éthanoïque, plus réactif :
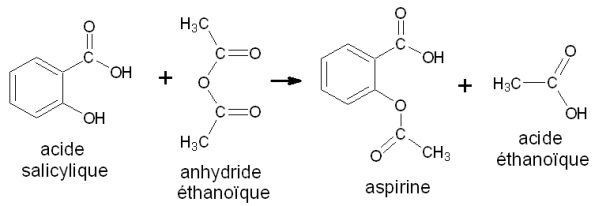
La réaction est lente, mais peut être accélérée par chauffage modéré. En Travaux pratiques, le montage correspondant se présente sous la forme :
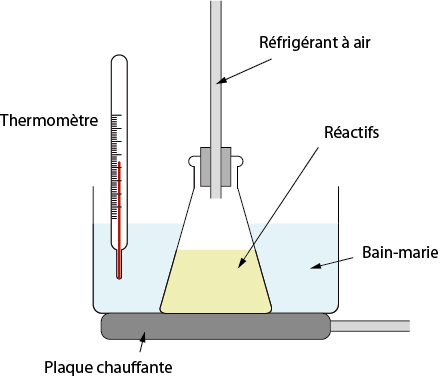
Pendant une vingtaine de minute, le mélange est maintenu à 60 °C par le bain marie. Un tube en verre fait office de réfrigérant à air, et condense les vapeurs afin qu’elles retombent dans le milieu réactionnel. L’acide sulfurique
Une fois la réaction terminée, le mélange est refroidi pour que l’aspirine cristallise, c'est-à-dire prenne une forme solide. Afin d’extraire les cristaux blancs formés, on utilise alors une filtration sous vide :
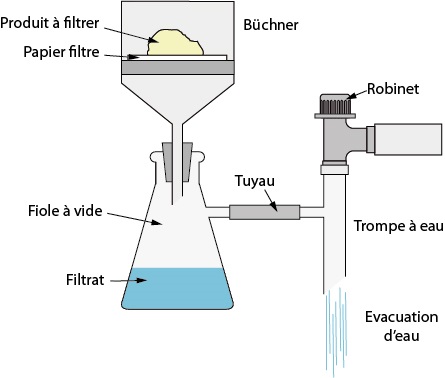
Le liquide passe à travers le papier filtre et à travers l’entonnoir Büchner, par gravité et par l’aspiration créée par la trompe à eau.
Afin de vérifier la qualité de l’aspirine synthétisée, il existe divers tests, comme une chromatographie sur couche mince (CCM). A partir de deux tâches étalons (acides salicylique et acétylsalicylique purs) et un échantillon de l’aspirine synthétisé, une CCM révélée sur UV peut donner ce résultat :
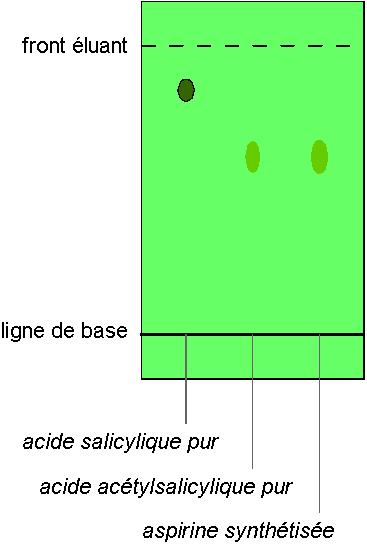
Dans cet exemple, l’aspirine synthétisée a été correctement purifiée, car elle ne fait pas apparaître des traces d’acide salicylique qui n’aurait pas réagi.
Remarque : l’acide salicylique est aussi synthétisable industriellement à partir du phénol, selon la réaction de Kolbe :
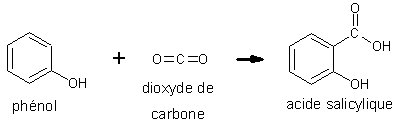
Le phénol est actuellement synthétisé majoritairement à partir du cumène, un produit pétrolier !
Une hémisynthèse se distingue par rapport à une synthèse par le fait que la molécule utilisée au départ est issue directement de substances naturelles et présente déjà quasiment la structure moléculaire de la molécule finale.
Par exemple, l’acide acétylsalicylique (l’aspirine) est produit par hémisynthèse, à partir de l’acide salicylique. Cette molécule présente des propriétés intéressantes en tant que médicament, qui sont conservées par l’aspirine, tout en étant moins nocive pour l’estomac. L’acide salicylique est une substance naturelle (saule), mais peut également être synthétisée à partir du phénol.
Certains critères sont à prendre en compte lors d’une synthèse ou hémisynthèse, comme le coût de fabrication de la molécule (réactifs, chauffage, rendement), l’aspect sécurité/environnement (toxicité de certaines espèces manipulées), ainsi qu’un contrôle qualité de l’espèce chimique produite (extraction, purification).

Des quiz et exercices pour mieux assimiler sa leçon
La plateforme de soutien scolaire en ligne myMaxicours propose des quiz et exercices en accompagnement de chaque fiche de cours. Les exercices permettent de vérifier si la leçon est bien comprise ou s’il reste encore des notions à revoir.

Des exercices variés pour ne pas s’ennuyer
Les exercices se déclinent sous toutes leurs formes sur myMaxicours ! Selon la matière et la classe étudiées, retrouvez des dictées, des mots à relier ou encore des phrases à compléter, mais aussi des textes à trous et bien d’autres formats !
Dans les classes de primaire, l’accent est mis sur des exercices illustrés très ludiques pour motiver les plus jeunes.

Des quiz pour une évaluation en direct
Les quiz et exercices permettent d’avoir un retour immédiat sur la bonne compréhension du cours. Une fois toutes les réponses communiquées, le résultat s’affiche à l’écran et permet à l’élève de se situer immédiatement.
myMaxicours offre des solutions efficaces de révision grâce aux fiches de cours et aux exercices associés. L’élève se rassure pour le prochain examen en testant ses connaissances au préalable.

Des vidéos et des podcasts pour apprendre différemment
Certains élèves ont une mémoire visuelle quand d’autres ont plutôt une mémoire auditive. myMaxicours s’adapte à tous les enfants et adolescents pour leur proposer un apprentissage serein et efficace.
Découvrez de nombreuses vidéos et podcasts en complément des fiches de cours et des exercices pour une année scolaire au top !

Des podcasts pour les révisions
La plateforme de soutien scolaire en ligne myMaxicours propose des podcasts de révision pour toutes les classes à examen : troisième, première et terminale.
Les ados peuvent écouter les différents cours afin de mieux les mémoriser en préparation de leurs examens. Des fiches de cours de différentes matières sont disponibles en podcasts ainsi qu’une préparation au grand oral avec de nombreux conseils pratiques.

Des vidéos de cours pour comprendre en image
Des vidéos de cours illustrent les notions principales à retenir et complètent les fiches de cours. De quoi réviser sa prochaine évaluation ou son prochain examen en toute confiance !








