Obtenir un spectre d'émission
- Fiche de cours
- Quiz et exercices
- Vidéos et podcasts
Obtenir expérimentalement le spectre d’une source lumineuse et l’interpréter à partir du diagramme de niveaux d’énergie des entités qui la constituent.
- On obtient le spectre d’émission de la lampe à l’aide d’un prisme qui servira à disperser les différentes raies colorées émises par la lampe.
- La mise sous tension de la lampe à vapeur de mercure fait passer les atomes d’un niveau haut en énergie vers un niveau plus bas en émettant un photon. Ce photon correspond à une radiation lumineuse.
- Le photon
- Énergie d’un photon
- Spectre de raies d'émission et d’absorption
- Quantification des niveaux d’énergie des atomes
Lorsqu’on soumet les atomes contenus dans une lampe à des décharges électriques, les atomes vont s’exciter en se positionnant dans des niveaux d’énergie supérieurs à l’état fondamental.
Peu de temps après, ils vont revenir sur le niveau le plus bas en perdant de l’énergie, ce qui se matérialise sous la forme de photons émis.
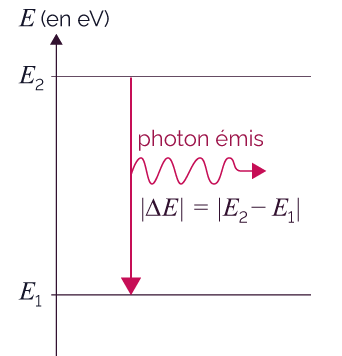
Émission d’un photon
Si l’atome permet plusieurs transitions différentes entre 3 états d’énergie ou plus, il y aura plusieurs longueurs d’onde différentes émises qui constitueront le spectre de raies brillantes.
Si un atome passe d’un état E3 à un état E1, 3 photons de 3 longueurs différentes sont émis.
Ces longueurs d’onde proviennent de :
- la transition d’un état d’énergie E2 vers un état d’énergie E1 ;
- la transition d’un état d’énergie E3 vers un état d’énergie E1 ;
- la transition d’un état d’énergie E3 vers un état d’énergie E2.
Le matériel nécessaire à la réalisation de cette expérience est le suivant.
- Une lampe à vapeur de mercure
- Un prisme
- Un écran
- Une fente
- Une lentille convergente
- Un banc d’optique
Le protocole pour obtenir le spectre d’émission est le suivant.
-
Mettre sous tension la lampe.
Brancher la lampe à vapeur de mercure au secteur. -
Focaliser les rayons.
On place ensuite sur le banc d’optique une fente suivie d’une lentille convergente pour focaliser les rayons émis par la lampe. -
Réaliser la dispersion du spectre
obtenu.
On positionne sur le trajet lumineux le prisme, qui est un élément dispersif. Il va servir à séparer les radiations émises pour obtenir le spectre d’émission de cette lampe. -
Récupérer le spectre.
On place un écran pour récupérer le spectre d’émission de cette lampe.
Le montage de l’expérience est le suivant.
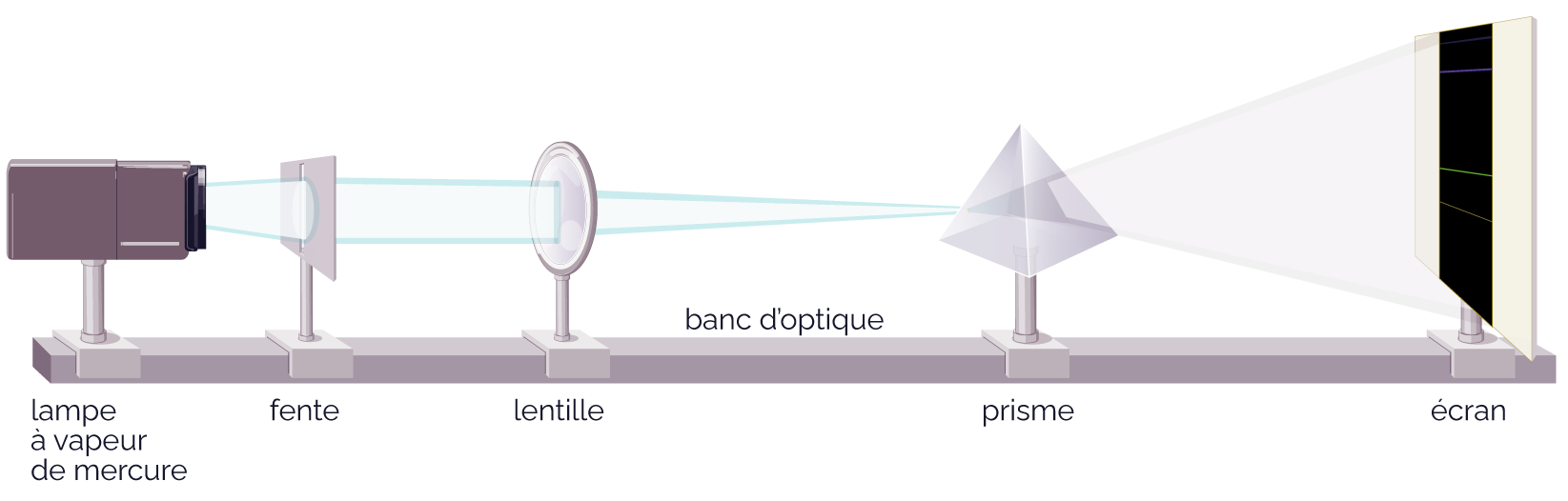
Schéma de l’expérience
Voici le spectre d’émission obtenu.
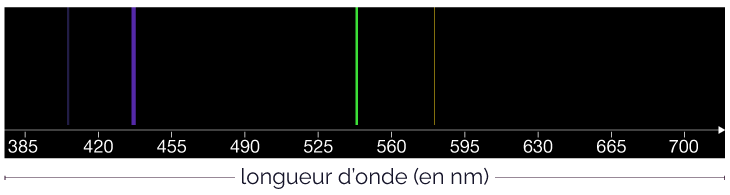
Spectre d’émission
La lampe à vapeur de mercure est une lampe spectrale constituée d’atomes de mercure sous forme de gaz.
Sa mise sous tension provoque des chocs entre les atomes. Les électrons de ces derniers passent alors sur des états excités.
Rapidement (typiquement 10−8 s), ils vont se désexciter puis émettre des photons qui correspondent aux diverses transitions possibles.
Certaines longueurs d’onde seront alors émises, ce qui constitue un spectre de raies brillantes.
Le spectre d’un atome est ainsi sa carte d’identité, il permet de l’identifier.
On observe sur l’écran 4 raies colorées qui se détachent sur un fond sombre : il s’agit bien d’un spectre d’émission.
La lampe à vapeur de mercure est donc une lampe polychromatique.
Ces raies colorées constituent la partie visible des raies émises par les atomes de mercure. Il existe d’autres raies lumineuses émises par cette lampe mais qui n’appartiennent pas au domaine du visible.
Chaque raie colorée correspond à une radiation monochromatique et à une transition énergétique d’un niveau haut en énergie vers un niveau plus bas.
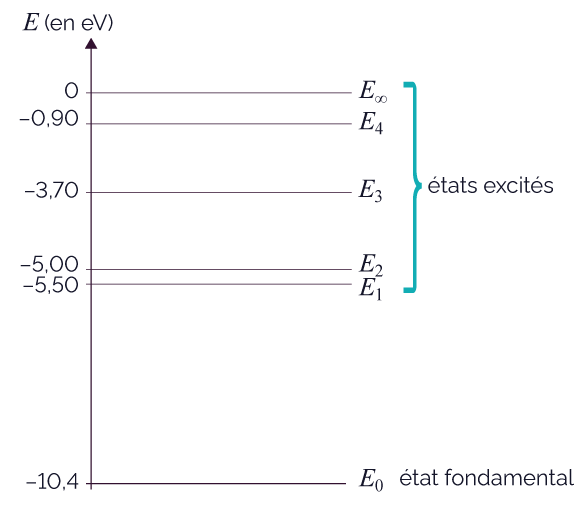
Diagramme d’énergie de l’atome de mercure
Par exemple, la transition du
niveau E4 vers le
niveau E3 correspond
à l’émission d’un photon
d’énergie |E4 − E3|
associée à la longueur
d’onde ![]() .
.
Comme l’énergie est en électronvolt (eV), il faut la convertir en Joule en la multipliant par 1,6 × 10−19.
On obtient alors :
![]()
λ = 439 nm.
C’est la deuxième raie (violette) du spectre d’émission de la lampe de mercure.

Des quiz et exercices pour mieux assimiler sa leçon
La plateforme de soutien scolaire en ligne myMaxicours propose des quiz et exercices en accompagnement de chaque fiche de cours. Les exercices permettent de vérifier si la leçon est bien comprise ou s’il reste encore des notions à revoir.

Des exercices variés pour ne pas s’ennuyer
Les exercices se déclinent sous toutes leurs formes sur myMaxicours ! Selon la matière et la classe étudiées, retrouvez des dictées, des mots à relier ou encore des phrases à compléter, mais aussi des textes à trous et bien d’autres formats !
Dans les classes de primaire, l’accent est mis sur des exercices illustrés très ludiques pour motiver les plus jeunes.

Des quiz pour une évaluation en direct
Les quiz et exercices permettent d’avoir un retour immédiat sur la bonne compréhension du cours. Une fois toutes les réponses communiquées, le résultat s’affiche à l’écran et permet à l’élève de se situer immédiatement.
myMaxicours offre des solutions efficaces de révision grâce aux fiches de cours et aux exercices associés. L’élève se rassure pour le prochain examen en testant ses connaissances au préalable.

Des vidéos et des podcasts pour apprendre différemment
Certains élèves ont une mémoire visuelle quand d’autres ont plutôt une mémoire auditive. myMaxicours s’adapte à tous les enfants et adolescents pour leur proposer un apprentissage serein et efficace.
Découvrez de nombreuses vidéos et podcasts en complément des fiches de cours et des exercices pour une année scolaire au top !

Des podcasts pour les révisions
La plateforme de soutien scolaire en ligne myMaxicours propose des podcasts de révision pour toutes les classes à examen : troisième, première et terminale.
Les ados peuvent écouter les différents cours afin de mieux les mémoriser en préparation de leurs examens. Des fiches de cours de différentes matières sont disponibles en podcasts ainsi qu’une préparation au grand oral avec de nombreux conseils pratiques.

Des vidéos de cours pour comprendre en image
Des vidéos de cours illustrent les notions principales à retenir et complètent les fiches de cours. De quoi réviser sa prochaine évaluation ou son prochain examen en toute confiance !








