Les verres et céramiques
- Fiche de cours
- Quiz et exercices
- Vidéos et podcasts
Le verre ordinaire est composé majoritairement de
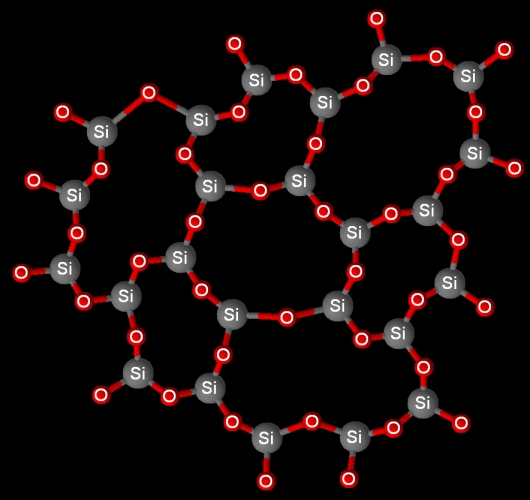
Le verre ordinaire est dur, cassant, isolant électrique. Il est quasi-inerte chimiquement. L’acide fluorhydrique HF peut toutefois le dissoudre. Sa masse volumique est
Production du verre
Le verre est produit par chauffage à 1500 °C d’un mélange de sable, de carbonate de sodium et de calcaire. Sous l’effet de la chaleur, la silice cristalline
Ensuite, si le milieu est refroidi assez vite, l’état amorphe est conservé lors de la solidification du verre. On parle de transition vitreuse pour désigner ce passage liquide/solide sans changement de l’état de la matière, sans recristallisation. Un rôle de matériaux mélangés au sable (fondants) est de perturber la structure du
Des additifs sont capables donner une couleur au verre. Il s’agit d’oxydes : oxydes de manganèse pour le violet, de nickel pour du gris, de chrome/fer pour du vert, de cobalt pour du bleu. D’autres matériaux ajoutés peuvent s’incorporer à la structure du verre, en lui donnant certaines propriétés, comme vu au 2.
Remarques :
→ Ce processus de fabrication du verre est une vitrification. Ce terme englobe aussi le fait qu’un matériau soit liquéfié à hautes températures puis refroidi rapidement pour conserver une structure amorphe. Par extension, le matériau ainsi vitrifié est qualifié de verre. La vitrification de roches est par exemple observée lors d’explosions nucléaires. La vitrification de déchets radioactifs désigne l’opération où ils sont piégés dans une structure vitreuse, afin d’éviter leur dissémination accidentelle dans la Nature.
→ Le verre peut être refondu, sans perte de ses propriétés. Dans le cadre de son recyclage, la consommation d’énergie est moindre que pour sa fabrication, car on ne monte plus alors à 1500 °C mais à 1000 °C.
→ Le verre pyrex comporte environ 80 % de
→ Un verre en « cristal » a pour composition massique : environ la moitié de
→ Pour les fibres de verre, la composition du verre est par exemple 55 % de
→ En optique, le verre est très employé, par exemple avec les fibres optiques. On utilise aussi le pouvoir dispersif de certains verres, avec les prismes. On rappelle qu’un milieu est dispersif si la célérité d’une onde lumineuse dépend de sa longueur d’onde. Exemple : crown, flint, … Leur composition est relativement complexe ; en plus des éléments vus plus haut, on a du phosphore, germanium, fluor, etc.
Pour les lunettes de vue, on parle de verre minéral (le verre en
Certains verres sont photochromiques, c'est-à-dire qu’ils s’assombrissent de manière réversible quand ils sont exposés à la lumière (UV) :
• Pour les verres minéraux : rajout d’halogénures d’argent (ex : chlorure d’argent).
• Pour les verres organiques : couche de molécules photochromes, comme l’oxazine.
→ Le verre feuilleté résulte de la superposition de plusieurs couches de verre liées entre elles par un film en polymère (ex : polyvinyle de butyral). Le verre feuilleté n’éclate pas en cas de choc, mais il apparaît une structure en étoile très caractéristique. Il se forme une multitude de petits éclats dont une partie reste fixée à la vitre. Application : pare-brise automobile. Les verres blindés sont conçus selon ce principe: utilisation de verre et de polycarbonate pour des vitres de fortes épaisseurs, capables de stopper des balles d’armes à feu.
→ Les vitrocéramiques désignent un verre résultant d’une cristallisation contrôlée du matériau. Les microcristaux formés sont noyés dans une phase vitreuse. Le matériau est non transparent. Il présente une forte résistance mécanique, tolère de fortes températures et chocs thermiques. Les vitrocéramiques sont composées principalement de
La définition d’une céramique est très vaste, car elle concerne les matériaux solides non métalliques et inorganiques. Le chlorure de sodium et le diamant sont ainsi des céramiques, tout comme la terre cuite ou la porcelaine (sens premier de céramique) … Par la suite, il sera sous-entendu que nous parlerons des céramiques industrielles, nommées aussi céramiques techniques. Elles possèdent souvent une structure cristalline, mais ce n’est pas obligatoire : le verre ainsi est une catégorie de céramique. On distingue deux ensembles :
• les oxydes :
• les non oxydes : carbures (carbone + autre élément chimique), borure (carbone + autre élément), nitrure (azote + autre élément) comme
Pour
Propriétés
Une céramique technique présente des propriétés physiques particulièrement intéressantes :
• Grande rigidité mécanique : le module de Young d’une céramique peut être plus fort que celui d’un métal.
• « Fragilité » : au contraire d’un métal, une céramique ne possède pas de zone plastique en traction (voir fiche sur les matériaux composites) : elle cassera plus tôt.
• Ténacité globalement plus faible que celle d’un métal. La ténacité est la faculté d’un matériau à résister à la propagation d’une fissure.
• Les céramiques sont plus résistantes en compression qu’en traction.
• Insensible à la corrosion, bonne résistance à l’usure.
• Inerte chimiquement.
• Température de fusion souvent élevée (
• Les céramiques sont fréquemment isolantes thermiques et électriques. Toutefois, certaines sont supraconductrices à très basses températures.
Exemple de céramique : Alumine
Fabrication d’une céramique
De fait des températures de fusion élevées des céramiques, elles sont très difficiles à mettre en forme par chauffage : on ne peut pas les fondre comme les métaux.
Une technique pour fabriquer une pièce manufacturée en céramique est le frittage. Elle consiste à réduire en poudre le matériau utilisé. Ensuite, la poudre est déposée dans un moule et est comprimée. Le matériau est porté à une température suffisante pour que les grains se soudent entre eux, mais on reste en dessous de la température de fusion de la céramique.
Durant le frittage, l’espace entre les grains tend à se réduire. Sous l’effet des contraintes appliquées, les grains changent de forme. Une fois l’opération terminée, il demeure des pores au sein de la céramique : des pores ouverts (communiquant avec l’extérieur), et les pores fermés. Les pores influent sur les propriétés mécaniques du matériau : module de Young, fragilité à la traction et/ou à la propagation de fissures, propriétés de surface, etc.
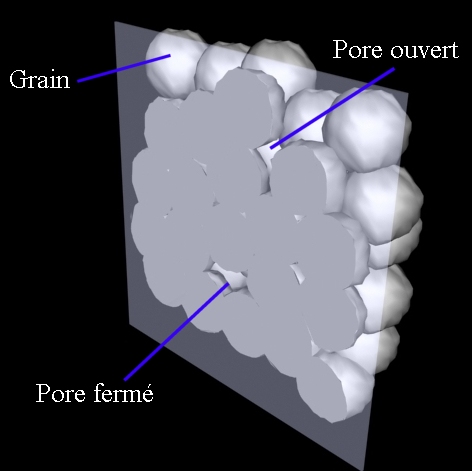
Le volume des pores ouverts s’obtient en comparant le volume géométrique
→ Pièces industrielles soumises à des contraintes thermiques et mécaniques importantes : soupapes, outils pour usinage du métal, …
→ Outils tranchants domestiques : couteaux ou ciseaux.
→ Matériaux réfractaires (résistants à la chaleur) : fours industriels, tuiles constituant le bouclier thermique des navettes spatiales.
→ Les propriétés isolantes des céramiques peuvent être mises à profit en électricité (hautes tensions) et en électronique.
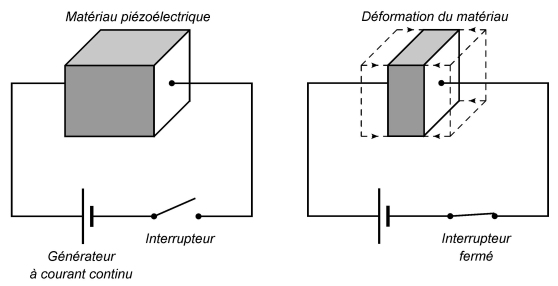
→ Céramiques piézoélectriques (fiche visualiser expérimentalement des atomes et des molécules). L’effet piézoélectrique est une déformation du matériau quand on lui applique une tension électrique, et inversement. Exemples : la céramique « PZT » (Titano-Zirconate de Plomb) ou le titianate de baryum
Les céramiques industrielles sont des matériaux non métalliques et inorganiques. Ils sont mis en forme par frittage. Ces matériaux possèdent des propriétés intéressantes pour des applications exigeantes : température de fusion élevée, grande résistance mécanique, insensibles à la corrosion…

Des quiz et exercices pour mieux assimiler sa leçon
La plateforme de soutien scolaire en ligne myMaxicours propose des quiz et exercices en accompagnement de chaque fiche de cours. Les exercices permettent de vérifier si la leçon est bien comprise ou s’il reste encore des notions à revoir.

Des exercices variés pour ne pas s’ennuyer
Les exercices se déclinent sous toutes leurs formes sur myMaxicours ! Selon la matière et la classe étudiées, retrouvez des dictées, des mots à relier ou encore des phrases à compléter, mais aussi des textes à trous et bien d’autres formats !
Dans les classes de primaire, l’accent est mis sur des exercices illustrés très ludiques pour motiver les plus jeunes.

Des quiz pour une évaluation en direct
Les quiz et exercices permettent d’avoir un retour immédiat sur la bonne compréhension du cours. Une fois toutes les réponses communiquées, le résultat s’affiche à l’écran et permet à l’élève de se situer immédiatement.
myMaxicours offre des solutions efficaces de révision grâce aux fiches de cours et aux exercices associés. L’élève se rassure pour le prochain examen en testant ses connaissances au préalable.

Des vidéos et des podcasts pour apprendre différemment
Certains élèves ont une mémoire visuelle quand d’autres ont plutôt une mémoire auditive. myMaxicours s’adapte à tous les enfants et adolescents pour leur proposer un apprentissage serein et efficace.
Découvrez de nombreuses vidéos et podcasts en complément des fiches de cours et des exercices pour une année scolaire au top !

Des podcasts pour les révisions
La plateforme de soutien scolaire en ligne myMaxicours propose des podcasts de révision pour toutes les classes à examen : troisième, première et terminale.
Les ados peuvent écouter les différents cours afin de mieux les mémoriser en préparation de leurs examens. Des fiches de cours de différentes matières sont disponibles en podcasts ainsi qu’une préparation au grand oral avec de nombreux conseils pratiques.

Des vidéos de cours pour comprendre en image
Des vidéos de cours illustrent les notions principales à retenir et complètent les fiches de cours. De quoi réviser sa prochaine évaluation ou son prochain examen en toute confiance !








