Établir la réaction de combustion
- Fiche de cours
- Quiz et exercices
- Vidéos et podcasts
- Citer des exemples de combustibles usuels.
- Écrire l’équation de réaction de combustion complète d’un alcane et d’un alcool.
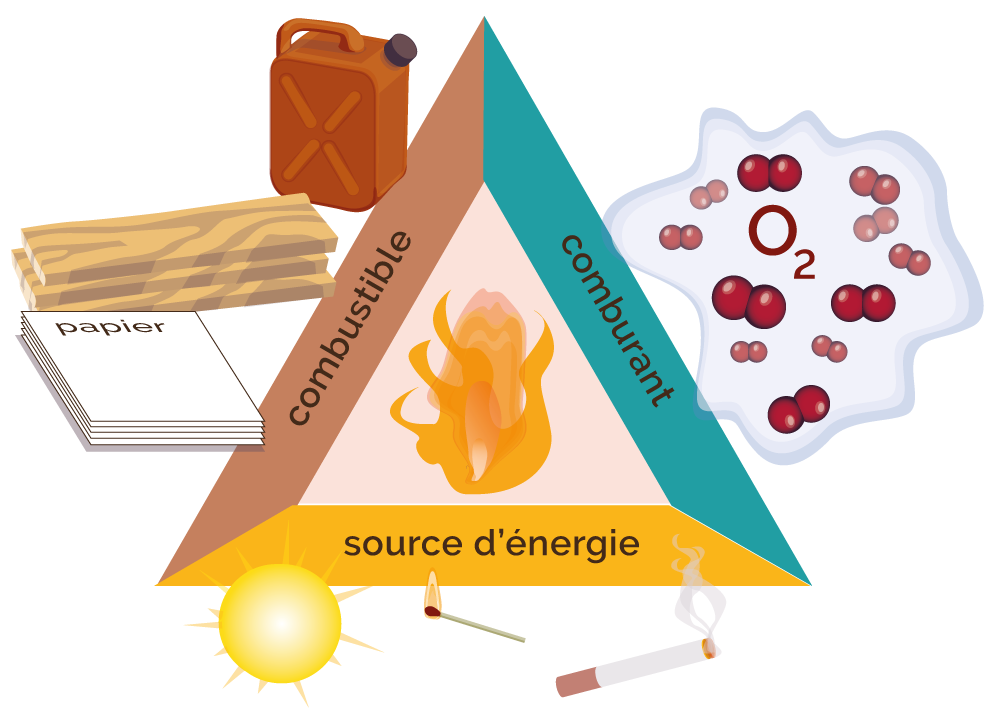
- Une combustion est une réaction chimique exothermique (qui dégage de la chaleur) qui met en jeu un combustible et un comburant. Une énergie doit être apportée pour activer la combustion.
- La combustion complète d’un hydrocarbure produit du dioxyde de carbone (CO2) et de l’eau (H2O).
- Équations et coefficients stœchiométriques
- Formule brute d’un alcool et d’un alcane
Cette réaction nécessite un apport d’énergie pour se produire : c’est l’énergie d’activation.
L’absence de l’un de ces 3 éléments empêche la combustion de se réaliser.
Quand il y a assez de dioxygène (excès), on dit que la combustion est complète. Les éléments carbone C, hydrogène H et parfois oxygène O réagissent entièrement et la réaction de combustion produit uniquement du dioxyde de carbone CO2 et de l’eau H2O sous forme gazeuse.
La combustion est un cas particulier de réaction d’oxydoréduction. On parle ici d’une réaction d’oxydoréduction par voie sèche car il n’y a pas de milieu aqueux.
De manière générale, une réaction d’oxydoréduction est une réaction qui se caractérise par un transfert d’électrons, d’un réducteur vers un oxydant. Le comburant est qualifié d’agent oxydant, le combustible s’oxyde donc et il y a un transfert d’électrons du comburant vers le combustible.
On distingue différents types de combustibles usuels.
- Les combustibles solides : le charbon, le bois, la paille, etc.
- Les combustibles liquides : les hydrocarbures (pétrole, essence, gazole, kérosène, fioul, etc.), les alcools (méthanol, éthanol, etc.), les esters (biodiesel).
- Les gaz : le méthane, le propane, le butane, etc.
Les combustibles fossiles contiennent essentiellement du carbone et proviennent des couches souterraines enfouies depuis des millions d’années.
On s’intéresse ici à la combustion des alcools et des alcanes, qui sont les combustibles organiques (combustibles fabriqués par les êtres vivants) les plus courants.
Pour écrire l’équation de la combustion d’un combustible, on respecte les étapes suivantes.
- Écrire la formule brute du combustible concerné.
- Écrire l’équation de la
combustion.
Pour écrire l’équation d’une combustion, on écrit :- les réactifs : le combustible et le comburant (dioxygène O2) à gauche de la flèche ;
- les produits : le dioxyde de carbone CO2 et l’eau H2O à droite de la flèche.
- Équilibrer l’équation de la
combustion.
Pour équilibrer l’équation, on ajoute les coefficients stœchiométriques devant les réactifs et les produits.
Il faut commencer par équilibrer les atomes de carbone, puis les atomes d’hydrogène et enfin les atomes d’oxygène.
De manière générale, l’équation de combustion d’un alcane CnH2n+2 sous forme gazeuse, solide ou liquide s’écrit de la manière suivante.
Le méthane est un gaz de ville.
- Il est composé de 1 atome de carbone,
donc n = 1.
Sa formule brute est CH4. - L’équation
non équilibrée de sa combustion
s’écrit :
CH4(g) + O2(g) → CO2(g) + H2O(g). - Une fois équilibrée,
l’équation de sa combustion
s’écrit donc :
CH4 + 2 O2(g) → CO2(g) + 2 H2O(g).
Le propane C3H8 est un gaz utilisé pour le chauffage.
- Il est composé de 3 atomes de
carbone, donc n = 3.
Sa formule brute est C3H8. - L’équation
non équilibrée de sa combustion
s’écrit :
C3H8(g) + O2(g) → CO2(g) + H2O(g). - Une fois équilibrée,
l’équation de sa combustion
s’écrit donc :
C3H8(g) + 5 O2(g) → 3 CO2(g) + 4 H2O(g).
De manière générale, l’équation de combustion d’un alcool CnH2n+2O s’écrit de la manière suivante.
L’éthanol est un solvant très utilisé dans la synthèse des médicaments mais aussi dans les biocarburants.
- La molécule d’éthanol est
composée de 2 atomes de carbone,
donc n = 2.
Sa formule brute est C2H6O. - L’équation
non équilibrée de sa combustion
s’écrit :
C2H6O(l) + O2(g) → CO2(g) + H2O(g). - Une fois équilibrée,
l’équation de sa combustion
s’écrit donc :
C2H6O(l) + 3 O2(g) → 2 CO2(g) + 3 H2O(g).
Le butanol est un solvant très utilisé pour les vernis et peintures.
- La molécule de butanol est composée
de 4 atomes de carbone, donc n = 4.
Sa formule brute est C4H10O. - L’équation
non équilibrée de sa combustion
s’écrit :
C4H10O(l) + O2 → CO2(g) + H2O(g). - Une fois équilibrée,
l’équation de sa combustion
s’écrit donc :
C4H10O(l) + 6 O2 → 4 CO2(g) + 5 H2O(g).

Des quiz et exercices pour mieux assimiler sa leçon
La plateforme de soutien scolaire en ligne myMaxicours propose des quiz et exercices en accompagnement de chaque fiche de cours. Les exercices permettent de vérifier si la leçon est bien comprise ou s’il reste encore des notions à revoir.

Des exercices variés pour ne pas s’ennuyer
Les exercices se déclinent sous toutes leurs formes sur myMaxicours ! Selon la matière et la classe étudiées, retrouvez des dictées, des mots à relier ou encore des phrases à compléter, mais aussi des textes à trous et bien d’autres formats !
Dans les classes de primaire, l’accent est mis sur des exercices illustrés très ludiques pour motiver les plus jeunes.

Des quiz pour une évaluation en direct
Les quiz et exercices permettent d’avoir un retour immédiat sur la bonne compréhension du cours. Une fois toutes les réponses communiquées, le résultat s’affiche à l’écran et permet à l’élève de se situer immédiatement.
myMaxicours offre des solutions efficaces de révision grâce aux fiches de cours et aux exercices associés. L’élève se rassure pour le prochain examen en testant ses connaissances au préalable.

Des vidéos et des podcasts pour apprendre différemment
Certains élèves ont une mémoire visuelle quand d’autres ont plutôt une mémoire auditive. myMaxicours s’adapte à tous les enfants et adolescents pour leur proposer un apprentissage serein et efficace.
Découvrez de nombreuses vidéos et podcasts en complément des fiches de cours et des exercices pour une année scolaire au top !

Des podcasts pour les révisions
La plateforme de soutien scolaire en ligne myMaxicours propose des podcasts de révision pour toutes les classes à examen : troisième, première et terminale.
Les ados peuvent écouter les différents cours afin de mieux les mémoriser en préparation de leurs examens. Des fiches de cours de différentes matières sont disponibles en podcasts ainsi qu’une préparation au grand oral avec de nombreux conseils pratiques.

Des vidéos de cours pour comprendre en image
Des vidéos de cours illustrent les notions principales à retenir et complètent les fiches de cours. De quoi réviser sa prochaine évaluation ou son prochain examen en toute confiance !








