Distinguer la nature physique, chimique ou nucléaire d'une transformation
- Fiche de cours
- Quiz et exercices
- Vidéos et podcasts
Distinguer la nature physique, chimique ou nucléaire d’une transformation à partir :
- de l’équation de la transformation ;
- des éléments conservés ou non lors de la transformation ;
- de la description de la transformation.
- Une transformation physique correspond à un changement d’état (solide, liquide ou gazeux) de la matière.
- Une transformation chimique est un « réarrangement » des éléments chimiques : il y a conservation des éléments chimiques, de la masse et des charges électriques.
- Une transformation nucléaire est une modification du noyau des atomes : il y a conservation des charges électriques mais modification des éléments chimiques et de la masse.
Les transformations physiques, chimiques et nucléaires
Une transformation physique correspond à un changement d’état (solide, liquide ou gazeux) de la matière.
Une transformation physique d’un corps pur est symbolisée par une équation de changement d’état dans laquelle on précise la formule du corps pur avec son état initial et son état final entre parenthèses.
Par convention, on écrit (s) pour l’état solide, (l) pour l’état liquide et (g) pour l’état gazeux.
L’équation de la fusion d’un corps de symbole X s’écrit :
X(s) → X(l)
L’équation de vaporisation d’un corps de symbole Y s’écrit :
Y(l) → Y(g)
La solidification de l’eau a pour équation : H2O(l) → H2O(s).
Les transformations physiques s’accompagnent d’un échange thermique avec l’extérieur.
- Les réactions de fusion, vaporisation et sublimation sont endothermiques : elles captent de l’énergie thermique.
- Les réactions de solidification, liquéfaction et condensation sont exothermiques : elles cèdent de l’énergie thermique.
Au cours d’une réaction chimique, il y a échange ou mise en commun d’électrons de valence des espèces chimiques présents initialement.
Seul le cortège électronique des atomes est mis en jeu lors d’une transformation chimique.
Une transformation chimique est schématisée par une équation de la forme suivante.
somme des réactifs → somme des produits
La combustion du propane est une transformation chimique qui transforme le propane et le dioxygène (les réactifs) en eau et dioxyde de carbone (les produits). Son équation chimique est : C3H8 + 5O2 → 3CO2 + 4H2O
Une transformation chimique peut être exothermique, endothermique ou athermique (pas de transfert d’énergie).
Généralement, les transferts thermiques des réactions chimique sont plus grands que ceux des transformations physiques
Des noyaux pères réarrangent leurs nucléons pour donner des noyaux fils.
Il n’y a donc pas de modification de la charge électrique (Z) ni du nombre de nucléons (A).
Cette perte de masse est due à l’énergie libérée par la réaction.
L’équation d’une transformation nucléaire fait apparaitre l’écriture conventionnelle des noyaux pères et fils, ainsi que des particules libres.
Une particule libre est une particule seule, qui peut être :
- un neutron de symbole
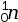 ;
;
- un électron de symbole
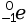 ;
;
- un positon de symbole
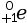 ;
;
- un proton de symbole
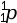 .
.
La réaction de fusion nucléaire des deux isotopes de l’hydrogène, le deutérium et le tritium, forme un atome d’hélium et libère un neutron. Son équation nucléaire est :
Beaucoup de transformations nucléaires sont très exothermiques. Pour une même masse de réactifs, une réaction nucléaire peut libérer environ 1 million de fois plus d’énergie qu’une réaction chimique.
Le tableau suivant rappelle ce qui est conservé en fonction du type de transformation.
| Transformation physique | Transformation chimique | Transformation nucléaire | |
| Conservation des espèces chimiques | × | ||
| Conservation des éléments chimiques (donc des noyaux) | × | × | |
| Conservation de la masse | × | × | |
| Conservation de la charge électrique | × | × | × |
| Conservation du nombre de nucléons | × | × | × |

Des quiz et exercices pour mieux assimiler sa leçon
La plateforme de soutien scolaire en ligne myMaxicours propose des quiz et exercices en accompagnement de chaque fiche de cours. Les exercices permettent de vérifier si la leçon est bien comprise ou s’il reste encore des notions à revoir.

Des exercices variés pour ne pas s’ennuyer
Les exercices se déclinent sous toutes leurs formes sur myMaxicours ! Selon la matière et la classe étudiées, retrouvez des dictées, des mots à relier ou encore des phrases à compléter, mais aussi des textes à trous et bien d’autres formats !
Dans les classes de primaire, l’accent est mis sur des exercices illustrés très ludiques pour motiver les plus jeunes.

Des quiz pour une évaluation en direct
Les quiz et exercices permettent d’avoir un retour immédiat sur la bonne compréhension du cours. Une fois toutes les réponses communiquées, le résultat s’affiche à l’écran et permet à l’élève de se situer immédiatement.
myMaxicours offre des solutions efficaces de révision grâce aux fiches de cours et aux exercices associés. L’élève se rassure pour le prochain examen en testant ses connaissances au préalable.

Des vidéos et des podcasts pour apprendre différemment
Certains élèves ont une mémoire visuelle quand d’autres ont plutôt une mémoire auditive. myMaxicours s’adapte à tous les enfants et adolescents pour leur proposer un apprentissage serein et efficace.
Découvrez de nombreuses vidéos et podcasts en complément des fiches de cours et des exercices pour une année scolaire au top !

Des podcasts pour les révisions
La plateforme de soutien scolaire en ligne myMaxicours propose des podcasts de révision pour toutes les classes à examen : troisième, première et terminale.
Les ados peuvent écouter les différents cours afin de mieux les mémoriser en préparation de leurs examens. Des fiches de cours de différentes matières sont disponibles en podcasts ainsi qu’une préparation au grand oral avec de nombreux conseils pratiques.

Des vidéos de cours pour comprendre en image
Des vidéos de cours illustrent les notions principales à retenir et complètent les fiches de cours. De quoi réviser sa prochaine évaluation ou son prochain examen en toute confiance !








