Distinguer les atomes, les molécules et les ions
- Fiche de cours
- Quiz et exercices
- Vidéos et podcasts
- Distinguer une molécule, un atome et un ion.
- Savoir interpréter et déterminer la formule d’une molécule ou d’un ion.
- Distinguer anion et cation.
- Un atome est électriquement neutre car le nombre d’électrons est égal au nombre de protons.
- Un atome qui a perdu des électrons est un ion monoatomique positif, appelé cation.
- Un atome qui a gagné des électrons est un ion monoatomique négatif, appelé anion.
- Une molécule est un assemblage
d’atomes.
Elle est électriquement neutre. - La formule chimique d’une molécule indique le symbole et le nombre des atomes qui la constituent.
Toute matière est constituée d’un
très grand nombre d’entités.
Ces entités sont des atomes,
des molécules ou des ions.
Toute matière est constituée à partir d’une infinité d’atomes.
Un atome est constitué d’un noyau, qui contient des protons (chargés +) et des neutrons (non chargés), autour duquel gravitent des électrons (chargés –).
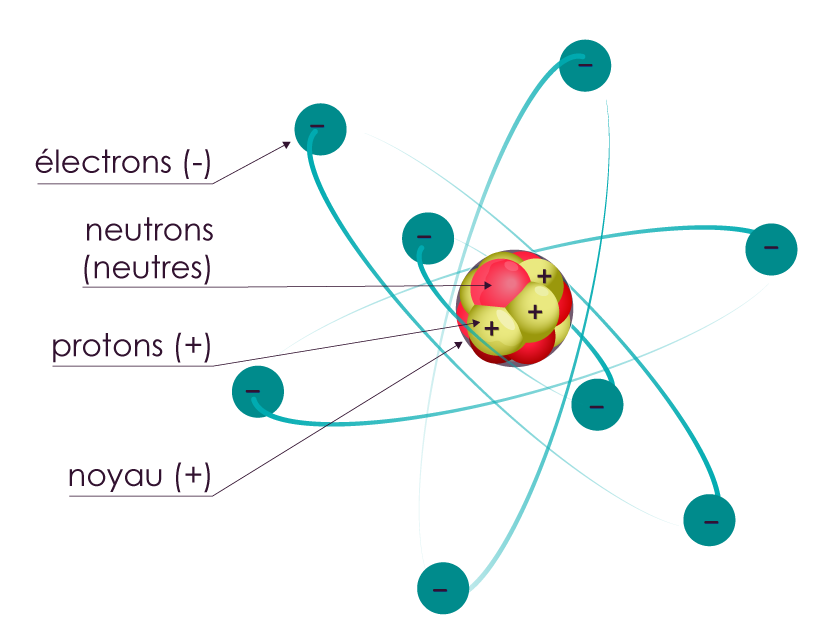
C’est le nombre de protons qui différencie deux atomes.
Chaque atome possède un nom et un symbole, répertoriés dans la classification périodique des éléments (ou tableau de Mendeleïev).
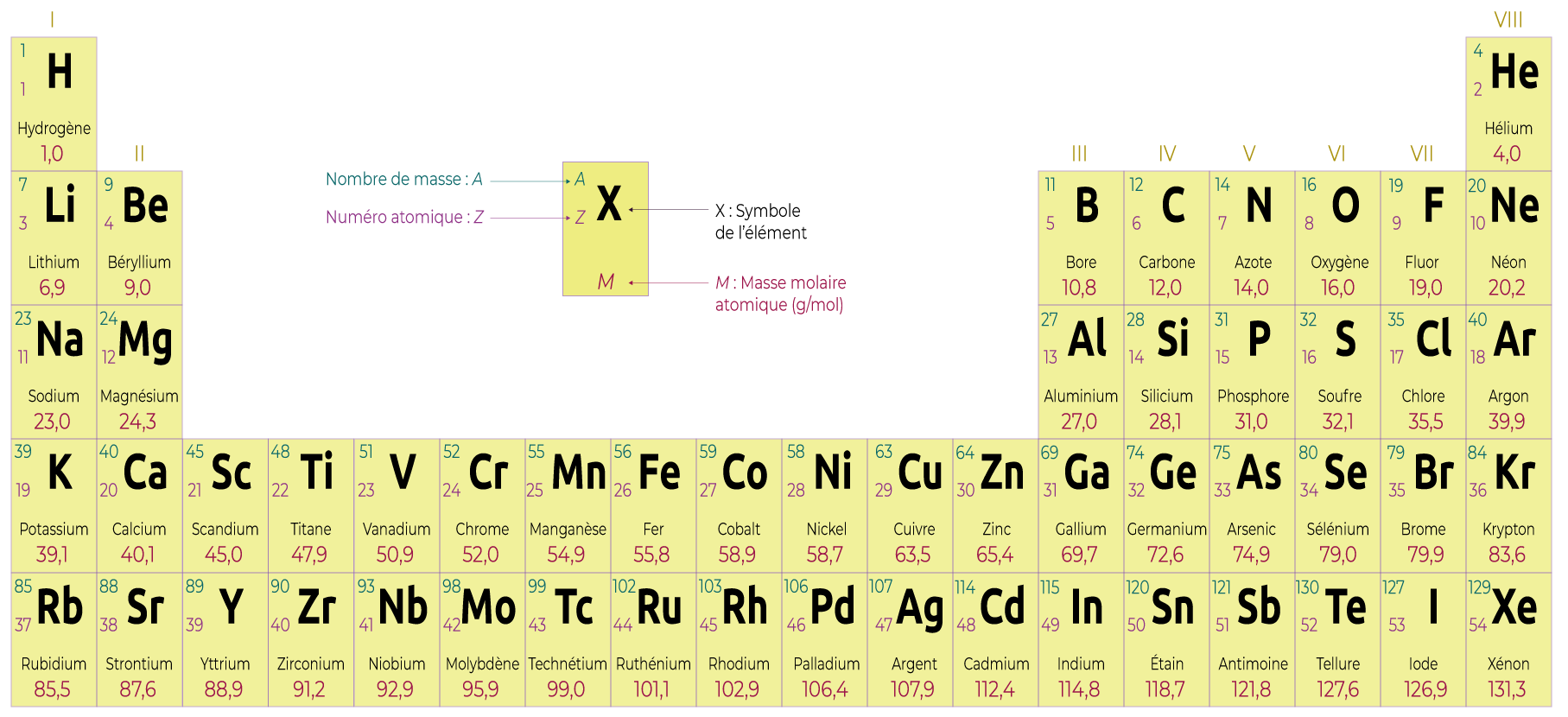
Classification périodique des éléments
La classification actuelle regroupe 118 atomes, dont 94 qui existent à l’état naturel sur Terre. Les autres atomes sont créés artificiellement en laboratoire et ont parfois une durée de vie très courte (de l’ordre de la microseconde : 10–6 s).
Le symbole du carbone est C, celui du chlore est Cl.
Un atome ou un groupement d’atomes a tendance à perdre ou gagner des électrons pour adopter la configuration la plus adaptée.
- positif ou plus commence par la lettre P comme perdu ;
- « cation » a plus (+) de lettres que « anion ».
Les ions formés à partir d’un seul atome sont des ions monoatomiques, tandis que ceux formés à partir de plusieurs atomes sont des ions polyatomiques. Le nombre d’électrons perdu(s) ou gagné(s) constitue la charge de l’ion.
- L’atome de sodium Na perd un électron et forme ainsi l’ion positif appelé sodium Na+ (cation). C’est un ion monoatomique.
- L’ion sulfate
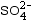 est un groupement
d’atomes de soufre et d’oxygène qui
a gagné 2 électrons. C’est un
ion polyatomique.
est un groupement
d’atomes de soufre et d’oxygène qui
a gagné 2 électrons. C’est un
ion polyatomique.
On attribue une formule brute à chaque molécule.
Une molécule est électriquement neutre.
- Une formule brute est écrite à partir du symbole de chaque sorte d’élément chimique présent dans la molécule.
- Les symboles des atomes sont dans l’ordre alphabétique, à l’exception des symboles C et H qui sont toujours placés dans cet ordre et en début de formule.
- Il faut ajouter un indice. Cet indice est un nombre, noté en bas à droite du symbole de l’atome, qui indique le nombre de chaque sorte d’atome.
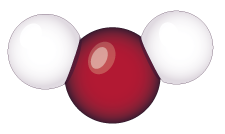
- La molécule d’eau est
constituée de deux atomes
d’hydrogène (symbole H) et
d’un atome d’oxygène
(symbole O).
La formule brute de l’eau est donc H2O.
L’élément H est suivi de l’indice 2, donc chaque molécule d’eau comporte deux atomes d’hydrogène.
L’élément O n’est suivi d’aucun indice, donc chaque molécule d’eau comporte un atome d’oxygène.
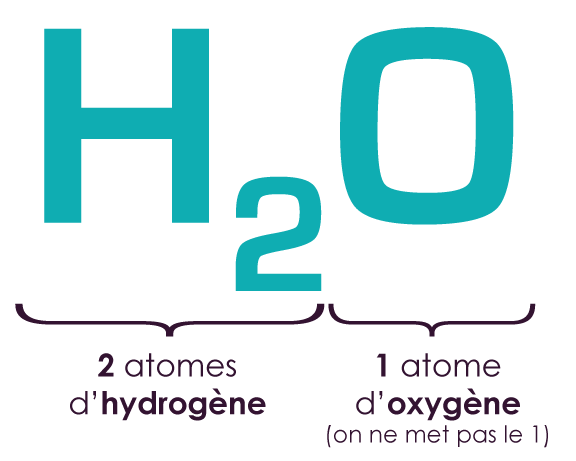
La formule chimique de l’eau - La molécule de butane a pour formule brute
C4H10.
Elle est constituée de 4 atomes de carbone et de 10 atomes d’hydrogène.
Le nom d’une molécule permet parfois de connaitre sa composition et donc de déterminer sa formule brute.
Dans la molécule de dioxygène par exemple, le préfixe « di » signifie deux. Une molécule de dioxygène est donc composée de deux atomes d’oxygène et sa formule brute est O2.
Les molécules peuvent être modélisées à l’aide de sphères colorées : c’est le modèle moléculaire.
Dans les modèles moléculaires, chaque atome est modélisé par une boule de couleur.
| Atome | Hydrogène | Carbone | Oxygène | Azote | Chlore |
| Modèle |

|
|

|
|
|
Voici les modèles moléculaires de quelques molécules de base.
| Nom | Formule | Modèle moléculaire |
| Diazote | N2 |

|
| Dioxygène | O2 |

|
| Eau | H2O |
|
| Dioxyde de carbone | CO2 |

|
| Méthane | CH4 |
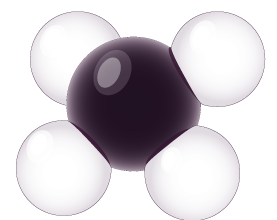
|
| Chlorométhane | CH3Cl |
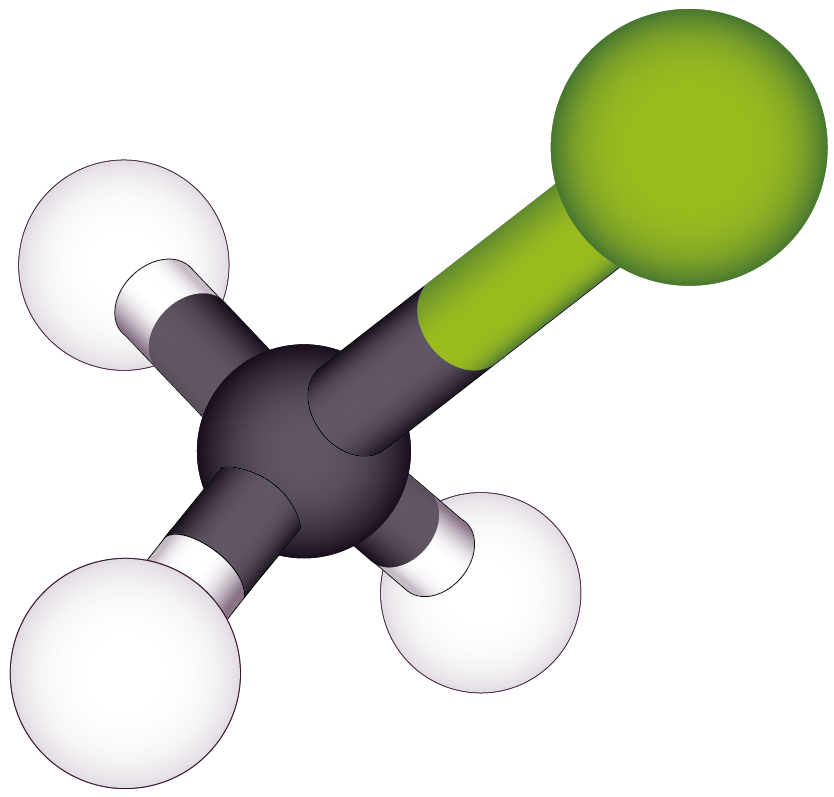
|

Des quiz et exercices pour mieux assimiler sa leçon
La plateforme de soutien scolaire en ligne myMaxicours propose des quiz et exercices en accompagnement de chaque fiche de cours. Les exercices permettent de vérifier si la leçon est bien comprise ou s’il reste encore des notions à revoir.

Des exercices variés pour ne pas s’ennuyer
Les exercices se déclinent sous toutes leurs formes sur myMaxicours ! Selon la matière et la classe étudiées, retrouvez des dictées, des mots à relier ou encore des phrases à compléter, mais aussi des textes à trous et bien d’autres formats !
Dans les classes de primaire, l’accent est mis sur des exercices illustrés très ludiques pour motiver les plus jeunes.

Des quiz pour une évaluation en direct
Les quiz et exercices permettent d’avoir un retour immédiat sur la bonne compréhension du cours. Une fois toutes les réponses communiquées, le résultat s’affiche à l’écran et permet à l’élève de se situer immédiatement.
myMaxicours offre des solutions efficaces de révision grâce aux fiches de cours et aux exercices associés. L’élève se rassure pour le prochain examen en testant ses connaissances au préalable.

Des vidéos et des podcasts pour apprendre différemment
Certains élèves ont une mémoire visuelle quand d’autres ont plutôt une mémoire auditive. myMaxicours s’adapte à tous les enfants et adolescents pour leur proposer un apprentissage serein et efficace.
Découvrez de nombreuses vidéos et podcasts en complément des fiches de cours et des exercices pour une année scolaire au top !

Des podcasts pour les révisions
La plateforme de soutien scolaire en ligne myMaxicours propose des podcasts de révision pour toutes les classes à examen : troisième, première et terminale.
Les ados peuvent écouter les différents cours afin de mieux les mémoriser en préparation de leurs examens. Des fiches de cours de différentes matières sont disponibles en podcasts ainsi qu’une préparation au grand oral avec de nombreux conseils pratiques.

Des vidéos de cours pour comprendre en image
Des vidéos de cours illustrent les notions principales à retenir et complètent les fiches de cours. De quoi réviser sa prochaine évaluation ou son prochain examen en toute confiance !








