Les transferts thermiques lors d'un changement d'état
- Fiche de cours
- Quiz et exercices
- Vidéos et podcasts
- Connaitre les termes exothermique et endothermique.
- Connaitre le signe d’une énergie thermique suivant le sens du transfert.
- Identifier le sens du transfert thermique lors d’un changement d’état et le relier au terme exothermique ou endothermique.
- Une transformation est dite exothermique si elle
s’accompagne d’une libération
d’énergie thermique.
C’est le cas des changements d’état dans lesquels les molécules deviennent moins agitées : solidification, liquéfaction et condensation. - Inversement, une transformation est dite
endothermique lorsqu’elle nécessite un apport
d’énergie pour se réaliser.
C’est le cas des changements d’état dans lesquels les molécules deviennent plus agitées : fusion, vaporisation et sublimation.
Les changements d’état de la matière et interprétations microscopiques
Il existe des transformations (physiques ou chimiques) qui s’accompagnent d’échanges d’énergie avec le milieu extérieur. Cette énergie peut être thermique, lumineuse, électrique, etc.
Cette chaleur libérée conduit à une augmentation de la température du système.
Les réactions de combustion sont des réactions exothermiques car elles s’accompagnent d’un dégagement de chaleur.
Faire bouillir de l’eau est une réaction endothermique car il est nécessaire de chauffer l’eau et donc de fournir de l’énergie pour que la vaporisation ait lieu.
La dissolution du sel (chlorure de sodium) dans l’eau est athermique car il n’y a ni dégagement, ni absorption de chaleur lorsque les ions Cl− et Na+ se dispersent dans l’eau.
L’énergie thermique, notée Q, se mesure en joule (J).
L’énergie thermique est une grandeur algébrique (avec un signe).
Le signe d’une énergie thermique dépend du sens du transfert, selon la convention suivante.
Une énergie thermique négative signifie que le système libère de la chaleur.

Transfert thermique d’une transformation exothermique
Une énergie thermique positive signifie que le système capte de la chaleur.

Transfert thermique d’une transformation endothermique
Les trois états physiques de la matière correspondent à des dispositions différentes des entités (atomes, molécules ou ions).
|
L’état solide correspond à une disposition ordonnée et compacte des entités. Les entités ne se déplacent pas mais vibrent sur place. |
 Modélisation de l’état solide |
|
L’état liquide correspond à une disposition désordonnée et compacte des entités. Les entités glissent les unes sur les autres. |
 Modélisation de l’état liquide |
|
L’état gazeux correspond à une disposition désordonnée et agitée des entités. Les entités ne sont pas en contact les unes avec les autres mais peuvent s’entrechoquer. |
 Modélisation de l’état gazeux |
Inversement, pour diminuer l’agitation des entités, celles-ci doivent céder de l’énergie.
Un changement d’état dans lequel l’agitation des entités augmente est endothermique, car le système reçoit de l’énergie.
Les changements d’état endothermiques sont la fusion, la vaporisation et la sublimation.
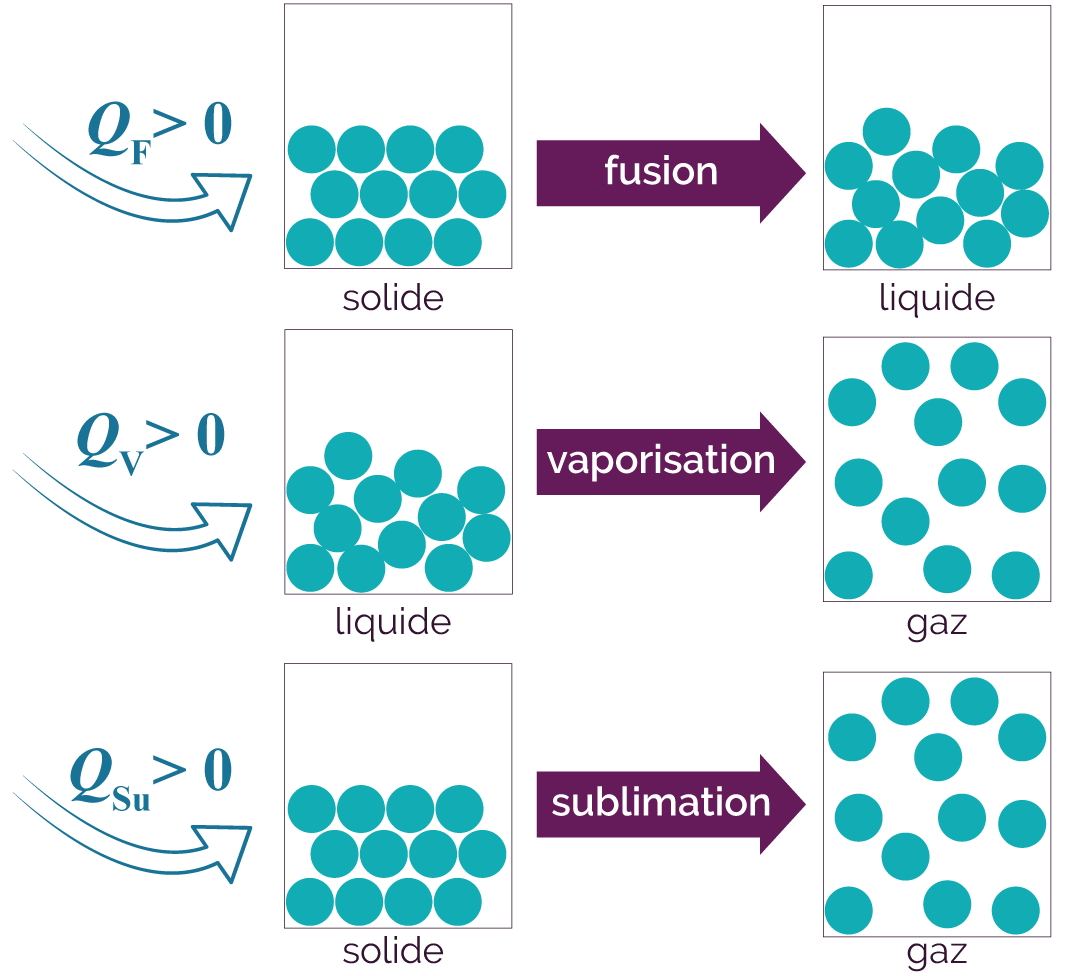
Changements d’état endothermiques
Un changement d’état dans lequel l’agitation des entités diminue est exothermique, car le système cède de l’énergie.
Les changements d’état exothermiques sont la solidification, la liquéfaction et la condensation.
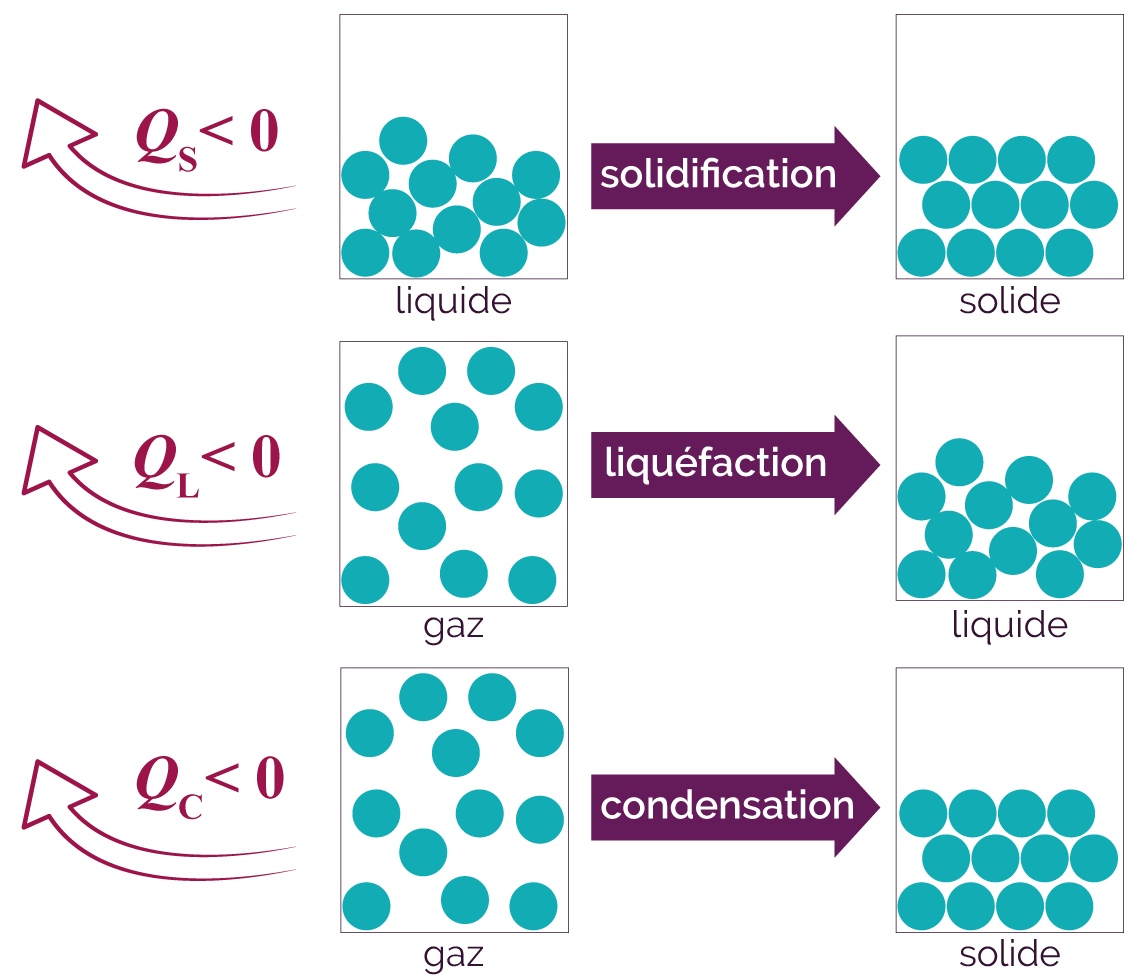
Changements d’état exothermiques
Les systèmes réfrigérants (réfrigérateurs, climatiseurs, etc.) exploitent le fait qu’en vaporisant un liquide (liquide frigorigène), le système capte de l’énergie à l’extérieur et donc le refroidit.

Des quiz et exercices pour mieux assimiler sa leçon
La plateforme de soutien scolaire en ligne myMaxicours propose des quiz et exercices en accompagnement de chaque fiche de cours. Les exercices permettent de vérifier si la leçon est bien comprise ou s’il reste encore des notions à revoir.

Des exercices variés pour ne pas s’ennuyer
Les exercices se déclinent sous toutes leurs formes sur myMaxicours ! Selon la matière et la classe étudiées, retrouvez des dictées, des mots à relier ou encore des phrases à compléter, mais aussi des textes à trous et bien d’autres formats !
Dans les classes de primaire, l’accent est mis sur des exercices illustrés très ludiques pour motiver les plus jeunes.

Des quiz pour une évaluation en direct
Les quiz et exercices permettent d’avoir un retour immédiat sur la bonne compréhension du cours. Une fois toutes les réponses communiquées, le résultat s’affiche à l’écran et permet à l’élève de se situer immédiatement.
myMaxicours offre des solutions efficaces de révision grâce aux fiches de cours et aux exercices associés. L’élève se rassure pour le prochain examen en testant ses connaissances au préalable.

Des vidéos et des podcasts pour apprendre différemment
Certains élèves ont une mémoire visuelle quand d’autres ont plutôt une mémoire auditive. myMaxicours s’adapte à tous les enfants et adolescents pour leur proposer un apprentissage serein et efficace.
Découvrez de nombreuses vidéos et podcasts en complément des fiches de cours et des exercices pour une année scolaire au top !

Des podcasts pour les révisions
La plateforme de soutien scolaire en ligne myMaxicours propose des podcasts de révision pour toutes les classes à examen : troisième, première et terminale.
Les ados peuvent écouter les différents cours afin de mieux les mémoriser en préparation de leurs examens. Des fiches de cours de différentes matières sont disponibles en podcasts ainsi qu’une préparation au grand oral avec de nombreux conseils pratiques.

Des vidéos de cours pour comprendre en image
Des vidéos de cours illustrent les notions principales à retenir et complètent les fiches de cours. De quoi réviser sa prochaine évaluation ou son prochain examen en toute confiance !








