Séparer les constituants d'un mélange homogène- Seconde- Physique Chimie
- Fiche de cours
- Quiz et exercices
- Vidéos et podcasts
- Connaitre des techniques de séparation des constituants d’un mélange homogène.
- Connaitre et savoir utiliser la verrerie adéquate.
- Les deux principales techniques de séparation des constituants d’un mélange homogène sont l’évaporation et la distillation.
- L’évaporation consiste à faire s’évaporer un liquide (généralement de l’eau) sous l’effet de la chaleur. Les autres constituants du mélange initial restent sous forme solide.
- La distillation consiste à faire passer une espèce parmi d’autres du mélange à l’état gazeux sous l’effet de la chaleur, puis à la faire se liquéfier (sous l’action d’un tube réfrigérant). Cette espèce est alors récupérée à la sortie du tube.
- Mélanges homogènes et mélanges hétérogènes
- Le matériel du chimiste – Verrerie
Pour rappel, un mélange homogène est un mélange dont on ne peut pas distinguer à l'œil nu les différents constituants.
On peut séparer les constituants d’un
mélange hétérogène par
décantation ou par filtration. C'est toutefois
impossible dans le cas d’un mélange
homogène car les éléments sont dissous
dans l’eau.
Pour séparer les différents constituants
d’un mélange homogène, on utilise
principalement deux techniques :
l'évaporation et la distillation.
On s’intéresse à de l’eau de mer, qui est salée. On ne peut pas distinguer à l’œil nu les cristaux de sel, il s’agit donc bien d’un mélange homogène.
On souhaite séparer le sel de l’eau de mer.
- On place une quantité d’eau de mer dans une boite en plastique sans couvercle.
- On pose cette boite au soleil pendant quelques heures. On obtient des cristaux de sel !
Quand toute l’eau contenue dans la boite s’évapore sous l’effet de la chaleur, le sel qui est dissous dans l’eau redevient solide et se dépose au fond de la boite.
L’eau peut en effet se transformer en vapeur d’eau mais pas le sel. On a donc séparé le sel de l’eau bien qu’il soit dissous dans l’eau.
- On peut accélérer le phénomène d'évaporation en chauffant l’eau.
- Ce phénomène peut s’observer
sur nos vêtements quand il fait chaud. Des
traces blanches apparaissent en effet sur notre
tee-shirt ou notre chemise après que
l’on ait transpiré et que nos
vêtements aient séchés. Ces
traces sont du sel !
La transpiration contient de l’eau et du sel (du sodium). Quand l’eau s’évapore sous l’effet de la chaleur et que nos vêtements sont alors secs, le sel qu’elle contient se dépose alors dessus.
La principale technique de séparation des constituants d’un mélange homogène s’appelle la distillation.
Le principe de la distillation est le suivant :
- Un mélange est chauffé dans un ballon.
- La partie liquide :
- se vaporise : elle passe de l'état liquide à l'état gazeux, à une température qui lui est propre,
- puis elle se condense (elle se liquéfie) dans un tube réfrigérant avant de s'écouler dans le bécher : c’est le distillat.
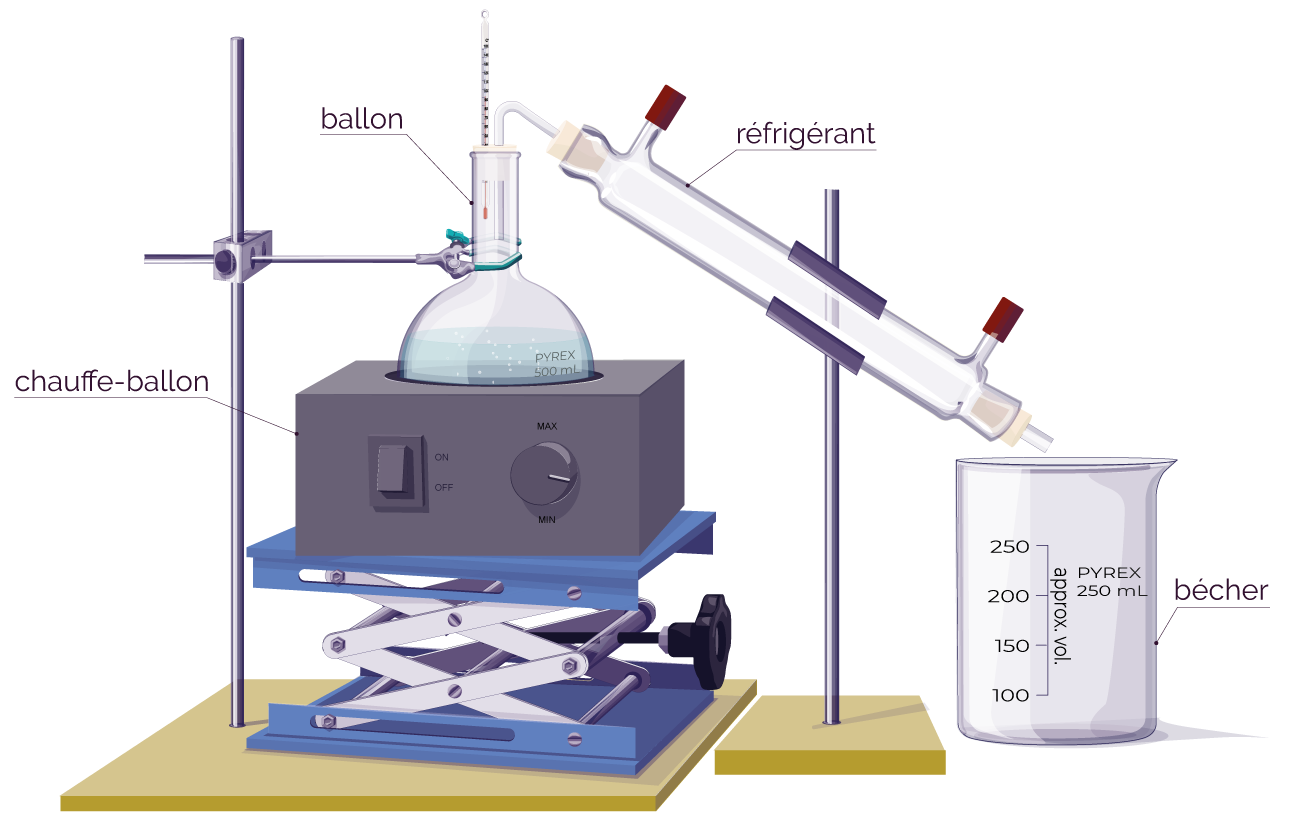
Montage pour la distillation
On utilise cette technique pour fabriquer l’eau distillée qu’on utilise en laboratoire. On distille pour cela de l’eau du robinet.
Deux cas sont possibles.
- Si on veut récupérer les solides
dissous dans un liquide : on chauffe le
liquide qui s’évapore mais pas les
solides.
À la fin de la distillation, on retrouve un dépôt au fond du ballon : c’est le résidu sec. C’est une technique peu employée car la « récolte » du résidu n’est pas toujours facile ! - Si on veut séparer deux liquides qui
constituent un mélange homogène : on
chauffe à une température précise,
ce qui provoque l’évaporation de
l’un des deux liquides.
En effet, chaque liquide possède une température d’ébullition (passage de l’état liquide à l’état gazeux) qui lui est propre.
Une eau minérale est une eau qui a dissous des
sels minéraux, lors de son passage dans le
sol.
Une eau minérale n'est pas un corps pur :
il s'agit d'un mélange homogène,
composé d'eau et de substances dissoutes :
les sels minéraux.
On souhaite distiller de l’eau minérale afin de recueillir l’eau en la séparant des sels minéraux.
L'eau est chauffée dans un ballon. Elle se vaporise, puis se condense dans un tube réfrigérant avant de s'écouler dans le bécher.
À la fin de la distillation, il s'est
formé un dépôt au fond du
ballon : le résidu sec, qui
contient les sels minéraux.
L'eau a bien été séparée
des sels minéraux : elle se trouve à
l'état liquide dans le bécher.

Des quiz et exercices pour mieux assimiler sa leçon
La plateforme de soutien scolaire en ligne myMaxicours propose des quiz et exercices en accompagnement de chaque fiche de cours. Les exercices permettent de vérifier si la leçon est bien comprise ou s’il reste encore des notions à revoir.

Des exercices variés pour ne pas s’ennuyer
Les exercices se déclinent sous toutes leurs formes sur myMaxicours ! Selon la matière et la classe étudiées, retrouvez des dictées, des mots à relier ou encore des phrases à compléter, mais aussi des textes à trous et bien d’autres formats !
Dans les classes de primaire, l’accent est mis sur des exercices illustrés très ludiques pour motiver les plus jeunes.

Des quiz pour une évaluation en direct
Les quiz et exercices permettent d’avoir un retour immédiat sur la bonne compréhension du cours. Une fois toutes les réponses communiquées, le résultat s’affiche à l’écran et permet à l’élève de se situer immédiatement.
myMaxicours offre des solutions efficaces de révision grâce aux fiches de cours et aux exercices associés. L’élève se rassure pour le prochain examen en testant ses connaissances au préalable.

Des vidéos et des podcasts pour apprendre différemment
Certains élèves ont une mémoire visuelle quand d’autres ont plutôt une mémoire auditive. myMaxicours s’adapte à tous les enfants et adolescents pour leur proposer un apprentissage serein et efficace.
Découvrez de nombreuses vidéos et podcasts en complément des fiches de cours et des exercices pour une année scolaire au top !

Des podcasts pour les révisions
La plateforme de soutien scolaire en ligne myMaxicours propose des podcasts de révision pour toutes les classes à examen : troisième, première et terminale.
Les ados peuvent écouter les différents cours afin de mieux les mémoriser en préparation de leurs examens. Des fiches de cours de différentes matières sont disponibles en podcasts ainsi qu’une préparation au grand oral avec de nombreux conseils pratiques.

Des vidéos de cours pour comprendre en image
Des vidéos de cours illustrent les notions principales à retenir et complètent les fiches de cours. De quoi réviser sa prochaine évaluation ou son prochain examen en toute confiance !








