Présenter et analyser un résultat
- Fiche de cours
- Quiz et exercices
- Vidéos et podcasts
- Écrire le résultat d’une mesure.
- Comparer un résultat à une valeur de référence.
- Appliquer la formule d'un écart relatif pour calculer sa valeur.
- Le résultat d’une mesure
s’écrit sous la forme : m ±
U unité, où :
- m est une mesure ou une moyenne ;
- et U = 2u où u est l’incertitude-type.
- La mesure est jugée satisfaisante si la valeur de référence est entre (m – U) et (m + U).
- L’incertitude-type u n’a qu’un seul chiffre significatif et m doit avoir le même nombre de chiffres après la virgule que u.
- Si l’incertitude u n’est pas
connue, on calcule l’écart relatif e
(en %).
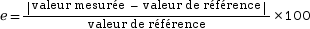
Si l’écart relatif est inférieur à 5 %, la mesure est satisfaisante.
- Calculer une incertitude-type
- Arrondis et chiffres significatifs
Le double de l’incertitude-type (2u) sera noté U (majuscule) et se nomme l’incertitude de la mesure.
Le résultat d’une mesure doit comporter obligatoirement :
- la valeur mesurée ou la valeur moyenne m ;
- l’incertitude U = 2u où u est l’incertitude-type ;
- l’unité.
Le résultat d’une mesure s’écrit sous la forme : m ± U unité
Une mesure de résistance s’écrit R = (150,3 ± 0,4) Ω, avec la mesure m = 150,3 et l’incertitude U = 0,4.
On suit la logique suivante pour arrondir la valeur mesurée m et l’incertitude U :
- On limite le nombre de chiffres significatifs à un seul chiffre significatif pour l’incertitude U, laquelle est arrondie à la valeur supérieure si nécessaire.
- Le dernier chiffre significatif de la grandeur mesurée m est le chiffre qui a la même position que le chiffre significatif de l’incertitude.
On mesure une intensité et on obtient m = 6,45872 A.
La calculatrice ou le tableur nous donne une incertitude U = 0,0054896 A, on écrit donc U = 0,006 A (on ne garde qu’un seul chiffre significatif et on arrondit à la valeur supérieure).
On arrondit la mesure m = 6,45872 A au millième car l’incertitude est au millième.
On écrit donc (6,459 ± 0,006) A.
On suppose qu’une valeur de référence (par exemple, une valeur théorique) est attendue pour une mesure.
Si le résultat d’une mesure m est accompagné de son incertitude U, alors la mesure est jugée satisfaisante si la valeur de référence est entre (m – U) et (m + U).
La valeur théorique de g est 9,81 N/kg et une moyenne des mesures de la constante de gravité est g = 9,750,08 N/kg.
On a m = 9,75 N/kg et U = 0,08 N/kg, donc m – U = 9,67 N/kg et m + U = 9,83.
La valeur théorique de g (9,81 N/kg) est bien comprise entre 9,67 et 9,83 : cette mesure est donc satisfaisante.
Si l’incertitude u n’est pas connue, on calcule l’écart relatif e (en %).
Il se calcule avec la formule suivante.
![]()
|valeur mesurée – valeur de référence| est la valeur absolue de la différence (valeur mesurée – valeur de référence). C’est donc un nombre positif car l’on ne tient pas compte du signe de la différence.
|5 – 6| = 1
|8 – 3| = 5
|1 – 10| = 9
Plus l’écart relatif est petit, plus la mesure est jugée satisfaisante.
On compare une concentration mesurée C = 6,32 × 10–5 mol/L à une concentration théorique de 6 × 10–5 mol/L. L’écart relatif est

Des quiz et exercices pour mieux assimiler sa leçon
La plateforme de soutien scolaire en ligne myMaxicours propose des quiz et exercices en accompagnement de chaque fiche de cours. Les exercices permettent de vérifier si la leçon est bien comprise ou s’il reste encore des notions à revoir.

Des exercices variés pour ne pas s’ennuyer
Les exercices se déclinent sous toutes leurs formes sur myMaxicours ! Selon la matière et la classe étudiées, retrouvez des dictées, des mots à relier ou encore des phrases à compléter, mais aussi des textes à trous et bien d’autres formats !
Dans les classes de primaire, l’accent est mis sur des exercices illustrés très ludiques pour motiver les plus jeunes.

Des quiz pour une évaluation en direct
Les quiz et exercices permettent d’avoir un retour immédiat sur la bonne compréhension du cours. Une fois toutes les réponses communiquées, le résultat s’affiche à l’écran et permet à l’élève de se situer immédiatement.
myMaxicours offre des solutions efficaces de révision grâce aux fiches de cours et aux exercices associés. L’élève se rassure pour le prochain examen en testant ses connaissances au préalable.

Des vidéos et des podcasts pour apprendre différemment
Certains élèves ont une mémoire visuelle quand d’autres ont plutôt une mémoire auditive. myMaxicours s’adapte à tous les enfants et adolescents pour leur proposer un apprentissage serein et efficace.
Découvrez de nombreuses vidéos et podcasts en complément des fiches de cours et des exercices pour une année scolaire au top !

Des podcasts pour les révisions
La plateforme de soutien scolaire en ligne myMaxicours propose des podcasts de révision pour toutes les classes à examen : troisième, première et terminale.
Les ados peuvent écouter les différents cours afin de mieux les mémoriser en préparation de leurs examens. Des fiches de cours de différentes matières sont disponibles en podcasts ainsi qu’une préparation au grand oral avec de nombreux conseils pratiques.

Des vidéos de cours pour comprendre en image
Des vidéos de cours illustrent les notions principales à retenir et complètent les fiches de cours. De quoi réviser sa prochaine évaluation ou son prochain examen en toute confiance !








