Déterminer la couleur d'une solution à partir du spectre UV-visible
- Fiche de cours
- Quiz et exercices
- Vidéos et podcasts
- Connaitre le principe d’absorbance.
- Exploiter un spectre d’absorption.
- Expliquer ou prévoir la couleur d’une espèce en solution à partir de son spectre UV-visible.
- L’absorbance A d’une solution
est une grandeur sans unité, elle représente
la quantité de lumière absorbée selon
la longueur d’onde
 de la lumière
traversée.
de la lumière
traversée.
- Un spectre UV-visible représente
l’absorbance A en fonction de la longueur
d’onde
 . Ce spectre présente un
pic pour une longueur d’onde donnée, qui
correspond à la couleur complémentaire de
la couleur de la solution.
. Ce spectre présente un
pic pour une longueur d’onde donnée, qui
correspond à la couleur complémentaire de
la couleur de la solution.
- Dispersion de la lumière blanche par un prisme
- Spectre de la lumière blanche
- Cercle des couleurs et couleurs complémentaires
La lumière est perçue par l’œil comme une couleur. Elle est cependant décomposée si on l’envoie sur un prisme.
Le visuel ci-dessous montre la décomposition à travers un prisme d’une lumière blanche émise par une lampe.
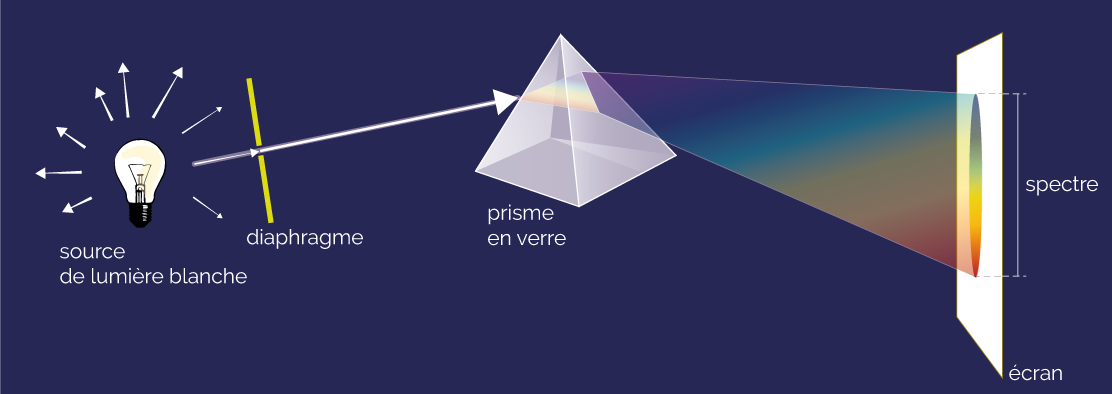
Décomposition d’une lumière blanche par un prisme

Spectre de la lumière blanche
La lumière blanche se décompose donc en une infinité de couleurs qui vont du violet au rouge. On dit que la lumière blanche est polychromatique.
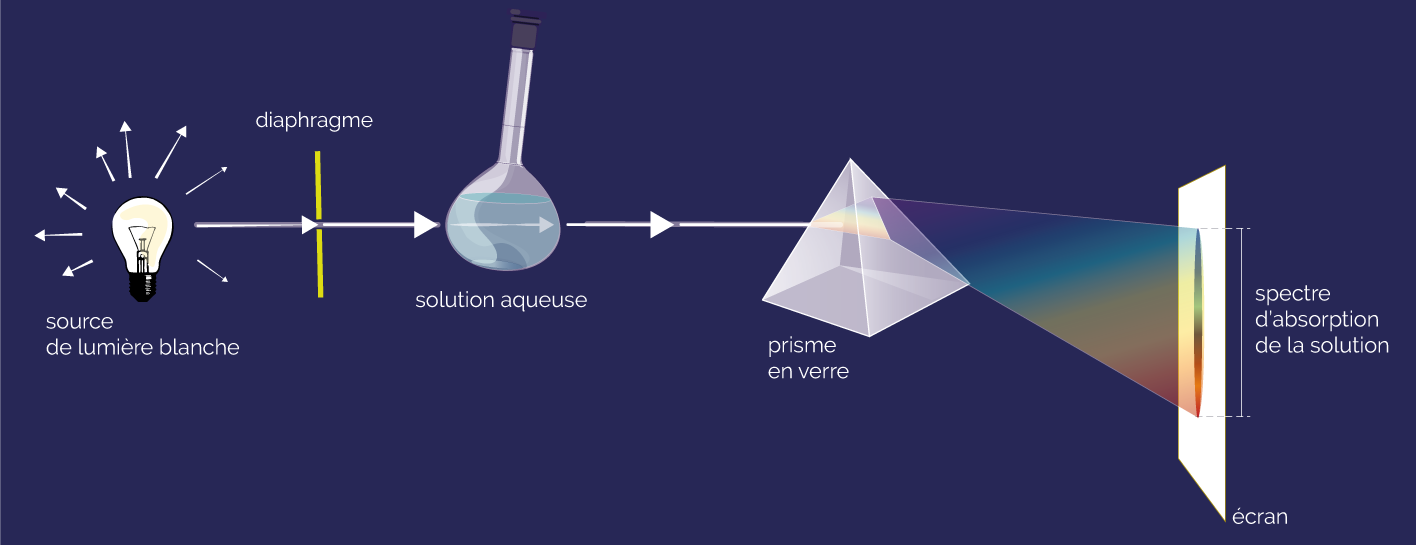
Spectre d’absorption d’une solution
Lorsque la lumière blanche traverse une solution aqueuse, certaines radiations présentes initialement sont absorbées. Le spectre obtenu présente des bandes noires appelées bandes d'absorption.
On compare le spectre d’absorption d’une solution aqueuse de permanganate de potassium au spectre de la lumière blanche.

Spectre d’absorption de la solution de permanganate de potassium
On observe que la solution de permanganate de potassium absorbe la couleur verte.
Les radiations absorbées dépendent des ions responsables de la couleur de la solution.
Une solution colorée absorbe une partie de la lumière qui la traverse.
L’absorbance A n’a pas d’unité, elle se mesure à l’aide d’un spectrophotomètre.

Spectrophotomètre
Pour les spectres UV-visibles, on utilise
habituellement les longueurs
d’onde ![]() suivantes.
suivantes.
- Dans l’UV : de 100 à 400 nm.
- Dans le visible : de 400 à 800 nm.
Pour chaque longueur d’onde ![]() , on mesure la valeur de
l’absorbance A de la solution.
, on mesure la valeur de
l’absorbance A de la solution.
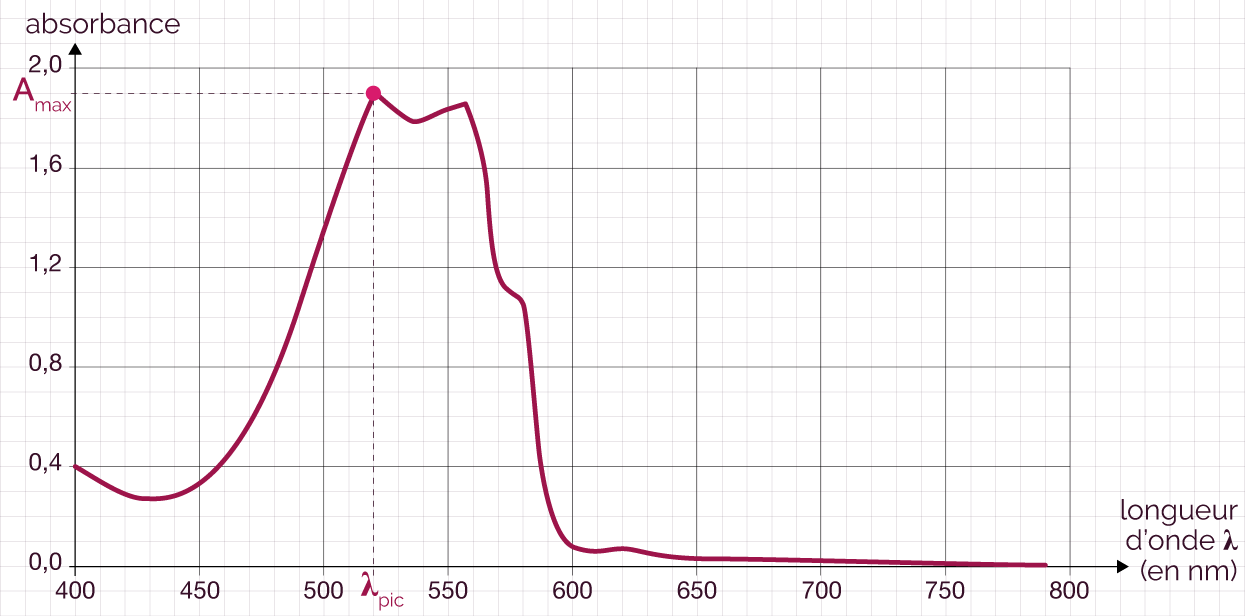
Courbe d’absorbance d’une solution de permanganate de potassium
On remarque sur le visuel ci-dessus que
l’absorbance A d’une solution
dépend de la longueur
d’onde ![]() de la lumière qui
la traverse.
de la lumière qui
la traverse.
Cette courbe présente un pic d’absorption
qui correspond à une
valeur Amax pour la longueur
d’onde ![]() .
.
La solution absorbe donc cette couleur ![]() et laisse passer toutes les
autres.
et laisse passer toutes les
autres.
La couleur de cette solution est alors le
complémentaire de la couleur
absorbée.
Sur la courbe d’absorbance d’une solution de permanganate de potassium ci-dessous, on observe que le maximum d’absorption de la solution de permanganate de potassium se situe autour de
Dans le cercle des couleurs ci-dessous, la couleur absorbée est située à l’opposé de la couleur complémentaire.
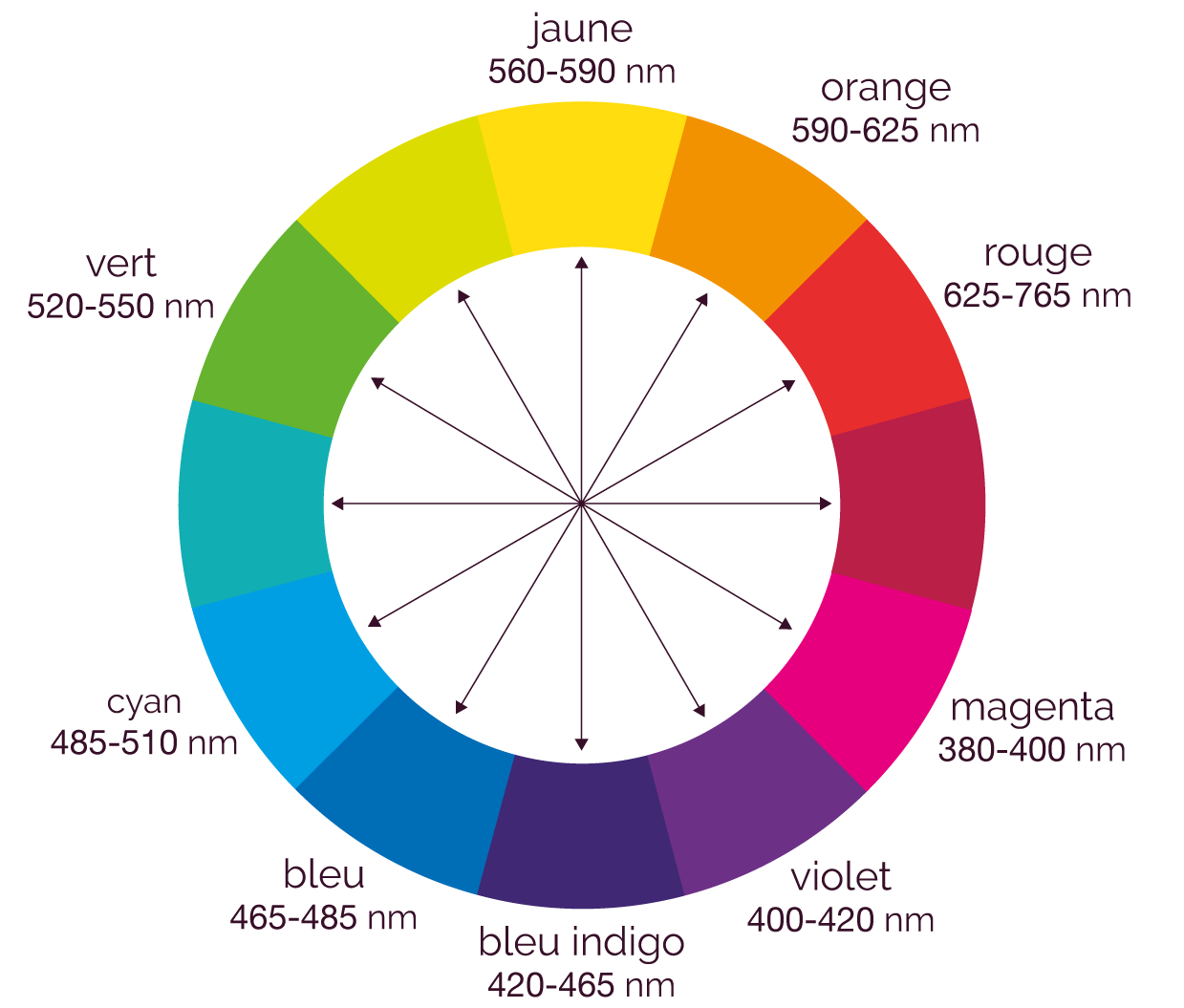
Cercle des couleurs
D’après ce cercle des couleurs, la
longueur d’onde ![]() = 520 nm
correspond au vert. Cette solution est donc magenta
(couleur complémentaire du vert).
= 520 nm
correspond au vert. Cette solution est donc magenta
(couleur complémentaire du vert).

Des quiz et exercices pour mieux assimiler sa leçon
La plateforme de soutien scolaire en ligne myMaxicours propose des quiz et exercices en accompagnement de chaque fiche de cours. Les exercices permettent de vérifier si la leçon est bien comprise ou s’il reste encore des notions à revoir.

Des exercices variés pour ne pas s’ennuyer
Les exercices se déclinent sous toutes leurs formes sur myMaxicours ! Selon la matière et la classe étudiées, retrouvez des dictées, des mots à relier ou encore des phrases à compléter, mais aussi des textes à trous et bien d’autres formats !
Dans les classes de primaire, l’accent est mis sur des exercices illustrés très ludiques pour motiver les plus jeunes.

Des quiz pour une évaluation en direct
Les quiz et exercices permettent d’avoir un retour immédiat sur la bonne compréhension du cours. Une fois toutes les réponses communiquées, le résultat s’affiche à l’écran et permet à l’élève de se situer immédiatement.
myMaxicours offre des solutions efficaces de révision grâce aux fiches de cours et aux exercices associés. L’élève se rassure pour le prochain examen en testant ses connaissances au préalable.

Des vidéos et des podcasts pour apprendre différemment
Certains élèves ont une mémoire visuelle quand d’autres ont plutôt une mémoire auditive. myMaxicours s’adapte à tous les enfants et adolescents pour leur proposer un apprentissage serein et efficace.
Découvrez de nombreuses vidéos et podcasts en complément des fiches de cours et des exercices pour une année scolaire au top !

Des podcasts pour les révisions
La plateforme de soutien scolaire en ligne myMaxicours propose des podcasts de révision pour toutes les classes à examen : troisième, première et terminale.
Les ados peuvent écouter les différents cours afin de mieux les mémoriser en préparation de leurs examens. Des fiches de cours de différentes matières sont disponibles en podcasts ainsi qu’une préparation au grand oral avec de nombreux conseils pratiques.

Des vidéos de cours pour comprendre en image
Des vidéos de cours illustrent les notions principales à retenir et complètent les fiches de cours. De quoi réviser sa prochaine évaluation ou son prochain examen en toute confiance !








