La loi d'Avogadro-Ampère et le volume molaire
- Fiche de cours
- Quiz et exercices
- Vidéos et podcasts
Dans ces conditions, quel volume occupe une mole de gaz ?
Revenons à la définition même de
l'état gazeux : c'est un état dispersé et
désordonné.
Les molécules de gaz ont un mouvement propre et elles
occupent tout le volume qu'elles ont à leur disposition.
La notion de pression se définit alors
comme l'ensemble des micro-chocs entre les
molécules et les parois qui limitent leur
déplacement.
La théorie d'Avogadro (1776-1856) indique que deux
volumes égaux de gaz différents,
pris dans les mêmes conditions de
température et de pression, contiennent
le même nombre de molécules c'est-à-dire la
même quantité de matière.
Par exemple, cela signifie qu'une mole de butane occupe le
même volume qu'une mole de dioxygène lorsque ces
deux gaz sont pris à la même pression et à la
même température
Cette théorie fait suite aux travaux de Dalton sur la
théorie atomique et de Gay-Lussac sur les proportions
volumiques.
Cette loi a des implications importantes car elle rend
possible la détermination de la masse molaire d'un gaz
à partir de celle d'un autre.
Mais, bien qu'André-Marie Ampère (1775-1836)
confirme cette hypothèse par une série
d'expériences ; les chimistes de l'époque,
pourtant plus enclins aux travaux empiriques, ne
reconnaîtront cette théorie que beaucoup plus tard.
Puisque la loi d'Avogadro-Ampère énonce qu'une mole
de n'importe quel gaz occupe toujours le même volume si
l'on travaille dans les mêmes conditions de
température et de pression, on peut connaître le
volume d'une mole de
gaz ou volume molaire
noté Vm.
Ainsi à 0°C et sous pression atmosphérique
normale (1013 hPa), le volume d'une mole de gaz est :
Vm = 22,4 L.mol-1.
Il est possible de trouver une relation entre quantité de matière, volume et volume molaire :
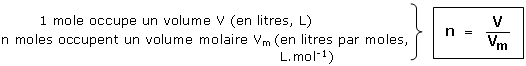
Remarque : cette relation est valable pour les solides et les liquides sous réserve de pouvoir déterminer leur volume molaire via la masse volumique et la masse molaire.
Par exemple : Pour déterminer le volume occupé par 0,3 moles de méthane de formule brute CH4 à 0°C et sous pression atmosphérique normale, il suffit d'utiliser :
V= n x Vm soit V = 0,3 x 22,4 = 6,72 L.
Notons bien que 0,3 moles de butane, de dioxygène, de
dihydrogène, occuperont le même volume !!!
Dans les mêmes conditions de température et de pression, tous les gaz ont le même volume molaire. A 0°C et sous pression atmosphérique normale, ce volume est : Vm = 22,4 L.mol-1.

Des quiz et exercices pour mieux assimiler sa leçon
La plateforme de soutien scolaire en ligne myMaxicours propose des quiz et exercices en accompagnement de chaque fiche de cours. Les exercices permettent de vérifier si la leçon est bien comprise ou s’il reste encore des notions à revoir.

Des exercices variés pour ne pas s’ennuyer
Les exercices se déclinent sous toutes leurs formes sur myMaxicours ! Selon la matière et la classe étudiées, retrouvez des dictées, des mots à relier ou encore des phrases à compléter, mais aussi des textes à trous et bien d’autres formats !
Dans les classes de primaire, l’accent est mis sur des exercices illustrés très ludiques pour motiver les plus jeunes.

Des quiz pour une évaluation en direct
Les quiz et exercices permettent d’avoir un retour immédiat sur la bonne compréhension du cours. Une fois toutes les réponses communiquées, le résultat s’affiche à l’écran et permet à l’élève de se situer immédiatement.
myMaxicours offre des solutions efficaces de révision grâce aux fiches de cours et aux exercices associés. L’élève se rassure pour le prochain examen en testant ses connaissances au préalable.

Des vidéos et des podcasts pour apprendre différemment
Certains élèves ont une mémoire visuelle quand d’autres ont plutôt une mémoire auditive. myMaxicours s’adapte à tous les enfants et adolescents pour leur proposer un apprentissage serein et efficace.
Découvrez de nombreuses vidéos et podcasts en complément des fiches de cours et des exercices pour une année scolaire au top !

Des podcasts pour les révisions
La plateforme de soutien scolaire en ligne myMaxicours propose des podcasts de révision pour toutes les classes à examen : troisième, première et terminale.
Les ados peuvent écouter les différents cours afin de mieux les mémoriser en préparation de leurs examens. Des fiches de cours de différentes matières sont disponibles en podcasts ainsi qu’une préparation au grand oral avec de nombreux conseils pratiques.

Des vidéos de cours pour comprendre en image
Des vidéos de cours illustrent les notions principales à retenir et complètent les fiches de cours. De quoi réviser sa prochaine évaluation ou son prochain examen en toute confiance !







