Les différents changements d'état de la matière
- Fiche de cours
- Quiz et exercices
- Vidéos et podcasts
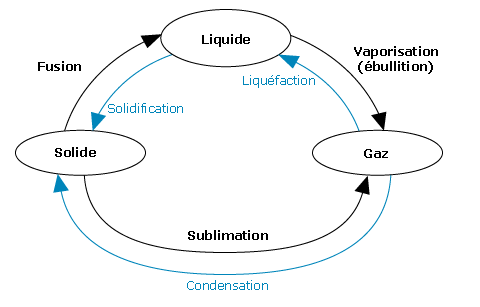
Les différents changements d'état portent des noms distincts, précisés dans le tableau ci-dessous :
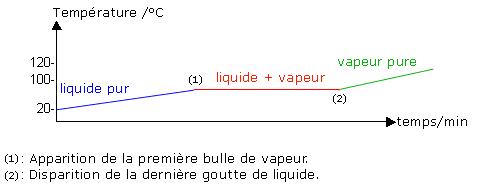
- Montée en température de l'eau liquide, de la
température initiale (20°C) à
100°C.
-
Stabilisation de la température à
100°C, de l'apparition de la
première bulle de vapeur à la disparition de la
dernière goutte de liquide (tout au long du changement
d'état).
- Montée en température de la vapeur d'eau jusqu'à la fin de l'expérience (120°C).
Cette expérience peut se résumer par la courbe suivante :
Lors du changement d'état, l'organisation spatiale des molécules est modifiée :
- par rupture de ces liaisons intermoléculaires : passage d'un état ordonné à un état moins ordonné lors des sublimation, fusion, vaporisation.
- ou par formation de ces liaisons, en augmentant la cohésion de la matière : passage d'un état désordonné à un état plus ordonné lors des liquéfaction, solidification, condensation.
- Si on fixe la pression, la température du changement
d'état est caractéristique du corps pur
considéré.
Exemple : Sous pression atmosphérique (1013 hPa), l'eau se vaporise à 100°C et se solidifie à 0°C. Le magnésium fond à 649°C et se vaporise à 1090°C.
- La mesure du point de fusion d'un solide ou du point
d'ébullition d'un liquide est donc un critère de
choix dans l'analyse d'un composé inconnu.
Exemple : Un liquide incolore inconnu peut être de l'eau, de l'éthanol ou de l'éther. La mesure de sa température d'ébullition sous pression atmosphérique est 78°C. On connaît les températures d'ébullition respectives de l'eau, de l'éthanol et de l'éther : 100°C, 78°C et 34°C. On déduit que le liquide inconnu est de l'éthanol.
- La température de changement d'état
dépendant de la pression, il est possible de modifier
cette dernière afin d'abaisser ou d'augmenter la
température.
Exemple : Dans un autocuiseur (P = 3 bar), l'ébullition de l'eau s'effectue à 125°C. Dans l'industrie, on réalise des évaporations de solvants sous pression réduite pour abaisser la température de vaporisation et ainsi réaliser des économies d'énergie.
Lorsqu'un corps pur change d'état physique, sa pression et sa température restent constantes pendant toute la durée du changement d'état.
Au cours d'un changement d'état, il se passe une modification des liaisons intermoléculaires et donc une modification de la cohésion de ce corps pur.
A pression donnée, la température de changement d'état d'un corps pur est une caractéristique du corps pur. La mesure de cette température permet donc de l'identifier.

Des quiz et exercices pour mieux assimiler sa leçon
La plateforme de soutien scolaire en ligne myMaxicours propose des quiz et exercices en accompagnement de chaque fiche de cours. Les exercices permettent de vérifier si la leçon est bien comprise ou s’il reste encore des notions à revoir.

Des exercices variés pour ne pas s’ennuyer
Les exercices se déclinent sous toutes leurs formes sur myMaxicours ! Selon la matière et la classe étudiées, retrouvez des dictées, des mots à relier ou encore des phrases à compléter, mais aussi des textes à trous et bien d’autres formats !
Dans les classes de primaire, l’accent est mis sur des exercices illustrés très ludiques pour motiver les plus jeunes.

Des quiz pour une évaluation en direct
Les quiz et exercices permettent d’avoir un retour immédiat sur la bonne compréhension du cours. Une fois toutes les réponses communiquées, le résultat s’affiche à l’écran et permet à l’élève de se situer immédiatement.
myMaxicours offre des solutions efficaces de révision grâce aux fiches de cours et aux exercices associés. L’élève se rassure pour le prochain examen en testant ses connaissances au préalable.

Des vidéos et des podcasts pour apprendre différemment
Certains élèves ont une mémoire visuelle quand d’autres ont plutôt une mémoire auditive. myMaxicours s’adapte à tous les enfants et adolescents pour leur proposer un apprentissage serein et efficace.
Découvrez de nombreuses vidéos et podcasts en complément des fiches de cours et des exercices pour une année scolaire au top !

Des podcasts pour les révisions
La plateforme de soutien scolaire en ligne myMaxicours propose des podcasts de révision pour toutes les classes à examen : troisième, première et terminale.
Les ados peuvent écouter les différents cours afin de mieux les mémoriser en préparation de leurs examens. Des fiches de cours de différentes matières sont disponibles en podcasts ainsi qu’une préparation au grand oral avec de nombreux conseils pratiques.

Des vidéos de cours pour comprendre en image
Des vidéos de cours illustrent les notions principales à retenir et complètent les fiches de cours. De quoi réviser sa prochaine évaluation ou son prochain examen en toute confiance !







