Les applications de la chromatographie
- Fiche de cours
- Quiz et exercices
- Vidéos et podcasts
• chromatographie d’encres ;
• chromatographie de la caféine ;
• chromatographie d’un colorant alimentaire ;
• chromatographie de la teneur en alcool du sang.
Pour cela on choisit soit un support poreux, soit une phase stationnaire ou fixe : ici, le papier.
Les encres à analyser sont placées en bas de ce support sur une ligne de référence juste au-dessus du niveau de la phase mobile.
b. Elution
Par contre les encres vertes et marrons sont bien séparées par l’eau :
vert = jaune + bleu ;
marron = rouge + jaune + bleu.
Mais le gris et le noir ne sont pas aussi bien séparés, il faudrait choisir un autre solvant et recommencer l’expérience.
Manipulation :
Soient 3 échantillons dissous dans
l’acétate d’éthyle :
• La caféine ;
• une pommade P ;
• un médicament énergisant
A.
Ils sont placés à la base d’une plaque de
chromatographie sur couche mince (CCM).
L’éluant est un mélange 9/1 d’acétate d’éthyle et d’éthanol très volatile donc il faudra recouvrir le bécher.
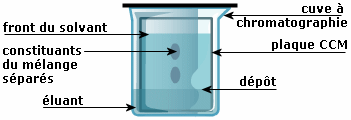
Après élution, la révélation se fait par absorption UV (ultraviolets) pour mettre en évidence ces substances incolores :
Exploitation :
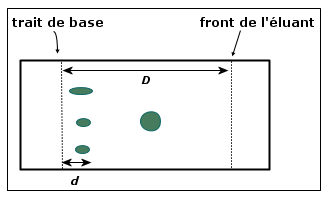
La caféine n’a migré qu’en une seule tache donc c’est une espèce pure, non un mélange. Le rapport frontal qui la caractérise vaut : Rf = 0,8/3,6 = 0,2.
On retrouve la même tache au même
Rf pour le médicament A et la pommade P
donc tous deux contiennent la caféine
identifiée par comparaison.
Le médicament A est un
mélange de plusieurs espèces
puisque son chromatogramme contient plusieurs
taches.
Manipulation :
Un morceau de coton est placé en bas de la pipette servant de colonne à la phase stationnaire (alumine solide et solution saturée de chlorure de sodium) : l’éluant (solution saturée de chlorure de sodium) imprègne lentement la colonne d’alumine en étant poussé par la pipette.
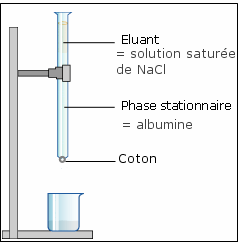
On dépose ensuite en haut de la colonne
le colorant vert qui pénètre
l’alumine. On rajoute de
l’éluant au fur et à mesure de la
descente pour que l’alumine ne soit jamais
sèche.
On recueille ainsi des fractions
colorées en changeant de bécher
régulièrement. 2 béchers sont
récupérés : l’un contenant une
solution jaune, l’autre une solution
bleue.
Exploitation :
Pour identifier ces deux colorants jaune et bleu, on peut faire un tracé de leurs spectres d’absorption à l’aide d’un spectrophotomètre pour les longueurs d’onde visibles (350 à 750 nm) en prenant comme solution étalon une solution d’éluant.
On compare ensuite ces spectres à des spectres connus ce qui permet d’identifier le jaune ou colorant tartrazine E 102 et le bleu patenté E131 composant le colorant vert étudié.
Manipulation :
La chromatographie en phase gazeuse (CPG) est
utilisée par les laboratoires de la Gendarmerie
nationale pour déterminer le taux d’alcool
dans le sang d’un conducteur.
L’échantillon de sang est
dilué dans un étalon
interne : le 2-méthylpropan-2-ol de
concentration connue.
Ce mélange liquide est injecté
dans une petite chambre chauffée à une
température suffisante pour que le
liquide soit entièrement et rapidement
vaporisé.
A la sortie de cette chambre, appelée
injecteur, les espèces chimiques du
mélange sont entraînées par un
courant de gaz inerte, la phase mobile. Tandis
que la phase stationnaire contenue dans la colonne est, en
général, de la silice plus ou moins
modifiée.
Exploitation :
Sur le même principe que la CCM, chaque produit pur donne un pic sur le chromatogramme obtenu. Les premiers correspondent aux espèces qui migrent le plus vite. On peut ainsi déterminer l’espèce à partir de références pures sur le principe des rapports frontaux.
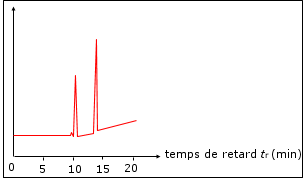
Le premier pic correspond à l’éthanol et le
second à l’étalon interne.
La seconde information donnée par la
CPG est l’aire du pic
correspondant à l’espèce à
détecter.
Grâce à une série d’étalons
d’éthanol de différentes
concentrations, on établie le graphique de
l’aire en fonction de la concentration et en reportant la
valeur de l’aire du pic on détermine la
concentration. Elle est, ici, de 1,7
g.L-1.
Mais la loi autorise une concetration maximale de
0,5g.L-1 depuis 2004. Donc le conducteur est
en infraction.
Les chromatographies font intervenir une phase stationnaire où sont déposés les échantillons, et une phase mobile qui entraîne les différents constituants à des vitesses différentes donc les sépare.
Les chromatographies de partage et d’adsorption permettent de déterminer la composition d’un mélange (papier ou CCM), de vérifier la composition d’un échantillon par comparaison avec des espèces pures mais aussi de quantifier la teneur en une espèce chimique précise par étalonnage.
Il est parfois nécessaire de révéler par procédé chimique (cristaux de diiode ou de permanganate) ou lumineux (UV) le chromatogramme lorsque les espèces sont incolores.

Des quiz et exercices pour mieux assimiler sa leçon
La plateforme de soutien scolaire en ligne myMaxicours propose des quiz et exercices en accompagnement de chaque fiche de cours. Les exercices permettent de vérifier si la leçon est bien comprise ou s’il reste encore des notions à revoir.

Des exercices variés pour ne pas s’ennuyer
Les exercices se déclinent sous toutes leurs formes sur myMaxicours ! Selon la matière et la classe étudiées, retrouvez des dictées, des mots à relier ou encore des phrases à compléter, mais aussi des textes à trous et bien d’autres formats !
Dans les classes de primaire, l’accent est mis sur des exercices illustrés très ludiques pour motiver les plus jeunes.

Des quiz pour une évaluation en direct
Les quiz et exercices permettent d’avoir un retour immédiat sur la bonne compréhension du cours. Une fois toutes les réponses communiquées, le résultat s’affiche à l’écran et permet à l’élève de se situer immédiatement.
myMaxicours offre des solutions efficaces de révision grâce aux fiches de cours et aux exercices associés. L’élève se rassure pour le prochain examen en testant ses connaissances au préalable.

Des vidéos et des podcasts pour apprendre différemment
Certains élèves ont une mémoire visuelle quand d’autres ont plutôt une mémoire auditive. myMaxicours s’adapte à tous les enfants et adolescents pour leur proposer un apprentissage serein et efficace.
Découvrez de nombreuses vidéos et podcasts en complément des fiches de cours et des exercices pour une année scolaire au top !

Des podcasts pour les révisions
La plateforme de soutien scolaire en ligne myMaxicours propose des podcasts de révision pour toutes les classes à examen : troisième, première et terminale.
Les ados peuvent écouter les différents cours afin de mieux les mémoriser en préparation de leurs examens. Des fiches de cours de différentes matières sont disponibles en podcasts ainsi qu’une préparation au grand oral avec de nombreux conseils pratiques.

Des vidéos de cours pour comprendre en image
Des vidéos de cours illustrent les notions principales à retenir et complètent les fiches de cours. De quoi réviser sa prochaine évaluation ou son prochain examen en toute confiance !







