Évolution historique de la composition de l'atmosphère
- Fiche de cours
- Quiz et exercices
- Vidéos et podcasts
La composition de l’atmosphère terrestre a beaucoup évolué depuis sa formation, il y a 4,5 milliards d’années, jusqu’à nos jours.
Comment cette composition a-t-elle évoluée ?
On suppose que l’agglomération (
accrétion) de poussières
chondritiques (poussières issues des
météorites) a donné naissance à la
Terre.
À partir de ces matériaux, la Terre a subi un
dégazage important qui a conduit à
la naissance d’une atmosphère primitive. La
gravitation terrestre est alors trop faible pour retenir
des gaz comme l’hélium et l’hydrogène
qui se dispersent dans l’espace.
L’étude des gaz recueillis lors
d’éruptions volcaniques ou la mesure de la
proportion des gaz contenus dans certaines
météorites permettent d’émettre des
hypothèses quant à la composition de
l’atmosphère primitive : on
présume qu'elle était constituée
essentiellement de vapeur d’eau, d’une
faible quantité de dioxyde de carbone et
de diazote, mais il n’y avait
pas de dioxygène.
L’atmosphère terrestre primitive est
réductrice (présence de
pyrite et de fer à l’état réduit).
Dès la fin de la phase
d’accrétion, la Terre connut un
refroidissement au cours duquel la
vapeur d’eau s'est condensée,
permettant ainsi la formation d’eau liquide à
l’origine des premiers océans.
Il s’en suivit une modification de la composition
de l’atmosphère : cette
dernière était alors essentiellement
formée de dioxyde de carbone,
CO2, de diazote,
N2, de
méthane, CH4 et
d’ammoniac,
NH3.
Aujourd’hui, les gaz qui composent
l’atmosphère sont, entre autres :
– le dioxygène : 20,8 % ;
– l’argon : 0,9 % ;
– le dioxyde de carbone : 0,03 %.
Le dioxygène présent dans l’atmosphère
provient de la photosynthèse.
L’évolution de la composition de
l’atmosphère est donc indissociable de la
présence des êtres vivants sur Terre.
Le passage de l’eau de l’état gazeux
à l’état liquide entraîne la
dissolution d’une grande partie du
CO2, sous forme d’ions
carbonates HCO3- , et sa
précipitation, à l’origine
de la formation des roches carbonatées
CaCO3 (réaction de
HCO3- avec Ca2+
lithosphérique).
Dès -3,8 Ga, la présence et surtout
l’activité de procaryotes
photosynthétiques (les
cyanobactéries, producteurs de
dioxygène) favorise la précipitation des
carbonates.
Les cyanobactéries captent les ions carbonates
présent dans les océans, qu’ils associent aux
ions calcium ; il en résulte la formation de dioxyde
de carbone, d’eau et d’un dépôt
calcaire :
2 HCO3- + Ca2+ → CO2 + CaCO3 + H2O.
• Le CO2 formé est piégé par les bactéries qui l’utilisent pour réaliser la photosynthèse.
– du dioxygène, O2, dégagé dans le milieu ;
À partir de - 3,5 Ga, la diversification des espèces photosynthétiques et leur prolifération, par une photosynthèse de plus en plus active, ont induit une fixation de plus en plus importante de CO2 et par conséquent, une libération accrue de dioxygène dans l’atmosphère.
Une partie de ce gaz s’est dissoute dans l’eau, mais, pour l’essentiel, le dioxygène s’est trouvé piégé dans des composés minéraux, abondants dans le domaine océanique. Les composés minéraux sont alors passés de l’état réduit à l’état oxydé.
Les abondants gisements d’oxydes de fer, datés de - 3,8 à - 2 Ga, témoignent de cette oxydation.
Après saturation du milieu marin (le dioxygène y a oxydé la majorité du fer disponible), l’apparition des premiers sols oxydés (présence de fers rubanées) vers - 2 Ga atteste de l’augmentation de la teneur en dioxygène dans l’atmosphère où il s’est accumulé progressivement.
La quantité de dioxygène atmosphérique n’a cessé de croître jusqu’à - 0,4 Ga. Cette augmentation est attribuée à la prolifération et à la diversification d’espèces photosynthétiques et à la faible consommation en O2 puisque le phénomène de la respiration apparaît plus tard (le dioxygène, toxique pour les êtres vivants anaérobies, favorise le développement de nouvelles espèces capables de l’utiliser et de libérer, par respiration, du dioxyde de carbone).
Ce déséquilibre, associé à la
fossilisation d’une partie de la matière
organique, a rendu possible cette accumulation de
dioxygène jusqu’à sa teneur
actuelle. Depuis, l’équilibre entre
production et consommation de dioxygène et de dioxyde de
carbone s’est instauré, permettant le
maintien d’une atmosphère
oxydante.
La présence de dioxygène dans la
haute atmosphère a progressivement permis la
formation d’une couche d’ozone
(O3), protectrice contre les UV, permettant
l’apparition, puis la
diversification d’une vie hors de
l’eau.
|
|
|
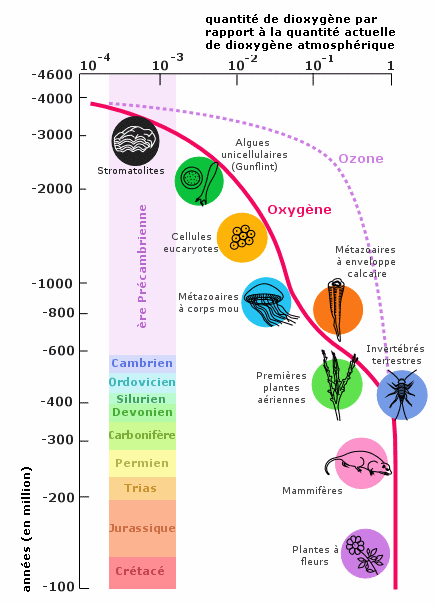
Doc. Évolution de la
quantité de dioxygène
atmosphérique |
L’atmosphère primitive a subi de multiples transformations, en relation avec l’évolution de la vie, qui ont donné naissance à l’atmosphère actuelle riche en O2.
L’atmosphère primitive s’est formée par dégazage. Elle était surtout constituée de vapeur d'eau, de dioxyde de carbone, CO2, et de diazote, N2, mais pas de dioxygène, O2.
La composition actuelle de l’atmosphère
(riche en N2 et O2) s’est mise en
place progressivement :
– la formation d’une hydrosphère liquide a
permis, par dissolution, de puiser le CO2
atmosphérique, puis de l’accumuler sous forme de
roches sédimentaires calcaires ; des conditions
favorables à l’apparition de la vie ont ainsi
été créées ;
– l’apparition des premiers êtres vivants
capables de photosynthèse a favorisé la
production de dioxygène. L’O2
libéré a immédiatement été
piégé et précipité sous forme
d’oxydes ; après épuisement des
matériaux réduits oxydables par le
dioxygène, son accumulation a pu se faire dans
l’atmosphère.
L’ensemble de ces phénomènes est à l’origine de la mise en place de conditions favorables au développement des organismes aérobies et à l’apparition de la vie hors de l’eau.

Des quiz et exercices pour mieux assimiler sa leçon
La plateforme de soutien scolaire en ligne myMaxicours propose des quiz et exercices en accompagnement de chaque fiche de cours. Les exercices permettent de vérifier si la leçon est bien comprise ou s’il reste encore des notions à revoir.

Des exercices variés pour ne pas s’ennuyer
Les exercices se déclinent sous toutes leurs formes sur myMaxicours ! Selon la matière et la classe étudiées, retrouvez des dictées, des mots à relier ou encore des phrases à compléter, mais aussi des textes à trous et bien d’autres formats !
Dans les classes de primaire, l’accent est mis sur des exercices illustrés très ludiques pour motiver les plus jeunes.

Des quiz pour une évaluation en direct
Les quiz et exercices permettent d’avoir un retour immédiat sur la bonne compréhension du cours. Une fois toutes les réponses communiquées, le résultat s’affiche à l’écran et permet à l’élève de se situer immédiatement.
myMaxicours offre des solutions efficaces de révision grâce aux fiches de cours et aux exercices associés. L’élève se rassure pour le prochain examen en testant ses connaissances au préalable.

Des vidéos et des podcasts pour apprendre différemment
Certains élèves ont une mémoire visuelle quand d’autres ont plutôt une mémoire auditive. myMaxicours s’adapte à tous les enfants et adolescents pour leur proposer un apprentissage serein et efficace.
Découvrez de nombreuses vidéos et podcasts en complément des fiches de cours et des exercices pour une année scolaire au top !

Des podcasts pour les révisions
La plateforme de soutien scolaire en ligne myMaxicours propose des podcasts de révision pour toutes les classes à examen : troisième, première et terminale.
Les ados peuvent écouter les différents cours afin de mieux les mémoriser en préparation de leurs examens. Des fiches de cours de différentes matières sont disponibles en podcasts ainsi qu’une préparation au grand oral avec de nombreux conseils pratiques.

Des vidéos de cours pour comprendre en image
Des vidéos de cours illustrent les notions principales à retenir et complètent les fiches de cours. De quoi réviser sa prochaine évaluation ou son prochain examen en toute confiance !