Détermination expérimentale du volume de base versé à l'équivalence
- Fiche de cours
- Quiz et exercices
- Vidéos et podcasts
Les courbes pH-métriques sont souvent utilisées donc leur étude sera approfondie.
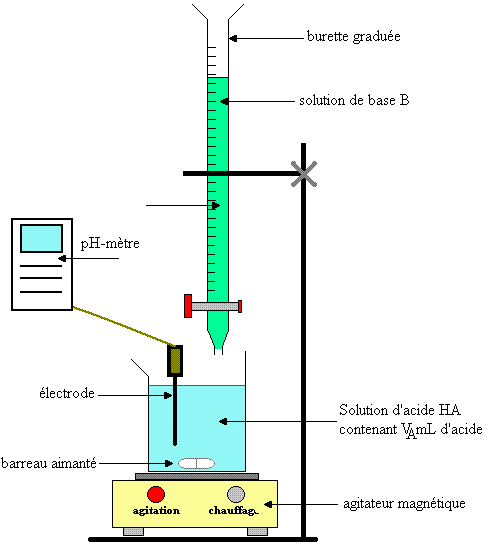
La burette doit être rincée
à l'eau distillée puis
avec la solution titrante avant d'être
remplie avec cette même solution jusqu'à la
graduation
« zéro » en
vérifiant le bas du ménisque et
l'absence d'air dans le tube sous le
robinet.
Attention à toujours placer un bécher
poubelle sous la burette graduée (en
cas de mauvaise manipulation ou de robinet
desserré).
Le titrage continue cependant bien après la passage à l'équivalence pour la détermination graphique de Ve.
Remarque : Pour que les électrodes trempent dans la solution on dilue avec de l'eau distillée le réactif titré ce qui ne modifie pas le nombre de moles ayant réagit.
Pour un dosage colorimétrique, il est conseillé de faire un premier dosage rapide pour déterminer grossièrement la valeur du volume équivalent puis un dosage plus précis en rapprochant les mesures à 1 mL avant l'équivalence retenue.
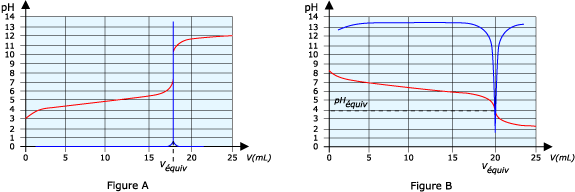
Pour le déterminer, une méthode graphique est facilement utilisée :
•tracer deux tangentes
parallèles à la courbe de
titrage au départ et à la fin du saut de
pH ;
•déterminer le milieu du segment
perpendiculaire à ces deux tangentes et tracer
la troisième parallèle
située à égale distance des deux
premières.
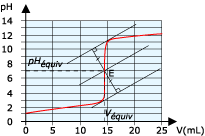
Cette méthode permet de déterminer sans calculs, le volume équivalent Ve et le pH à l'équivalence pHe par les coordonnées du point d'équivalence E.
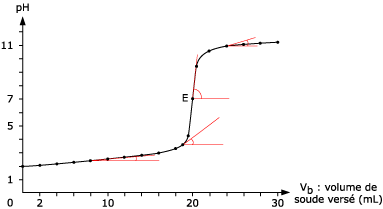
Le calcul de ce coefficient directeur k s'écrit :
•k = [pH(B) - pH(A)] / [VA(B) - VB(A)]
C'est-à-dire que pour une petite variation de volume ΔVB, on peut écrire que ce coefficient directeur est égal à la dérivée du pH en fonction du volume :
Cette méthode permet de déterminer avec un assistant de calculs, le volume équivalent Ve mais pas le pH à l'équivalence pHe.
Lors d'un titrage acido-basique :
•le volume VA de
réactif titré est placé
dans un bécher où on rajoute de
l'eau distillée si nécessaire
pour que les électrodes des appareils de mesures soient
en solution ;
•la solution titrante de concentration
connue CB est placée dans une
burette graduée.
Le suivi des caractéristiques pH et conductivité en fonction du volume de solution titrante versée donne des représentations graphiques qu'il faudra étudier pour déterminer le volume équivalent Ve.
Sur une courbe de titrage pH-métrique,
deux méthodes sont envisagées :
•méthode des tangentes, graphique,
qui permet de déterminer Ve et pHe ;
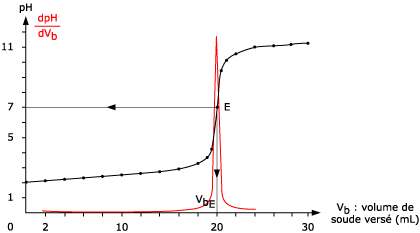
•méthode de la
dérivée, en calculant d pH /
d VB à chaque volume de solution
titrante versé et dont le maximum indiquera
Ve.

Des quiz et exercices pour mieux assimiler sa leçon
La plateforme de soutien scolaire en ligne myMaxicours propose des quiz et exercices en accompagnement de chaque fiche de cours. Les exercices permettent de vérifier si la leçon est bien comprise ou s’il reste encore des notions à revoir.

Des exercices variés pour ne pas s’ennuyer
Les exercices se déclinent sous toutes leurs formes sur myMaxicours ! Selon la matière et la classe étudiées, retrouvez des dictées, des mots à relier ou encore des phrases à compléter, mais aussi des textes à trous et bien d’autres formats !
Dans les classes de primaire, l’accent est mis sur des exercices illustrés très ludiques pour motiver les plus jeunes.

Des quiz pour une évaluation en direct
Les quiz et exercices permettent d’avoir un retour immédiat sur la bonne compréhension du cours. Une fois toutes les réponses communiquées, le résultat s’affiche à l’écran et permet à l’élève de se situer immédiatement.
myMaxicours offre des solutions efficaces de révision grâce aux fiches de cours et aux exercices associés. L’élève se rassure pour le prochain examen en testant ses connaissances au préalable.

Des vidéos et des podcasts pour apprendre différemment
Certains élèves ont une mémoire visuelle quand d’autres ont plutôt une mémoire auditive. myMaxicours s’adapte à tous les enfants et adolescents pour leur proposer un apprentissage serein et efficace.
Découvrez de nombreuses vidéos et podcasts en complément des fiches de cours et des exercices pour une année scolaire au top !

Des podcasts pour les révisions
La plateforme de soutien scolaire en ligne myMaxicours propose des podcasts de révision pour toutes les classes à examen : troisième, première et terminale.
Les ados peuvent écouter les différents cours afin de mieux les mémoriser en préparation de leurs examens. Des fiches de cours de différentes matières sont disponibles en podcasts ainsi qu’une préparation au grand oral avec de nombreux conseils pratiques.

Des vidéos de cours pour comprendre en image
Des vidéos de cours illustrent les notions principales à retenir et complètent les fiches de cours. De quoi réviser sa prochaine évaluation ou son prochain examen en toute confiance !







